Ты альдегиды и кетоны у них очень похожие органические функции. Оба имеют в своей структуре карбонильную функциональную группу (C = O) с той лишь разницей, что в случае альдегидов, он всегда появляется на конце углеродной цепи, то есть одним из карбонильных углеродных лигандов является водород; кетоны имеют карбонил между двумя другими атомами углерода.
Функциональная группа альдегидов:Функциональная группа кетонов:
О О
║ ║
C C ─ H С С ─ С
По этой причине существуют случаи функциональной изомерии между альдегидами и кетонами. Например, ниже мы представляем два функциональных изомера, которые имеют одинаковую молекулярную формулу (C3ЧАС6O), но один - альдегид (пропаналь), а другой - кетон (пропанон). Посмотрите, как это полностью меняет их свойства и применение:
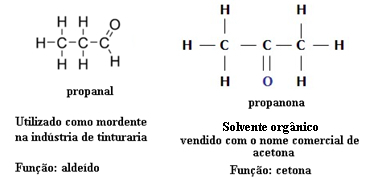
Пример функциональной изомерии альдегида и кетона
Представьте, что вы находитесь в лаборатории и обнаруживаете пузырек с бесцветной жидкостью, имеющей только молекулярную формулу C.3ЧАС6О. Что бы вы сделали, чтобы узнать, кетон это или альдегид?
Чтобы решить подобные проблемы, существуют методы дифференциации альдегидов и кетонов, основанные на реакции этих соединений со слабыми окислителями.. Как показано ниже, при столкновении со слабыми окислителями альдегиды реагируют путем окисления, в то время как кетоны не реагируют. Мы говорим чтоальдегиды действуют как восстановители, но кетоны не действуют., они реагируют только как восстановители при контакте с энергичными окислителями.
Альдегиды + Слабые окислители → карбоновая кислота
О О
║ ║
C ─ C ─ H + [O] → C ─ C ─ OH
Кетоны + Слабые окислители → Не реагируют
О
║
C ─ C ─ C + [O] → Никакой реакции не происходит
Исходя из этого, достаточно провести эту реакцию и посмотреть, реагирует ли соединение или нет. Если он реагирует, мы знаем, что это альдегид; если не реагирует, это кетон.
Кроме того, продукты, образующиеся в этих реакциях окисления альдегидов, хорошо видны с изменением цвета, как будет показано позже.
Существует три основных метода дифференциации альдегидов и кетонов:
1- Толленс реактивный: Этот реагент является аммиачный раствор нитрата серебра, т.е. он содержит нитрат серебра (AgNO3) и избыток гидроксида аммония (NH4ОЙ):
AgNO3 + 3 NH4ОН → Ag (NH3)ОЙ + NH4НА3 + 2 часа2О
Tollens Reactive (назван в честь немецкого химика Бернхарда Толленса (1841-1918))
Как объяснено в тексте Изготовление серебряного зеркала, когда альдегид вступает в контакт с реактивным Толленсом, он окисляется до соответствующей карбоновой кислоты, а ионы серебра восстанавливаются до Ag0 (серебристый металлик). Если эту реакцию проводить, например, в пробирке, это металлическое серебро будет осаждаться на стенках пробирки, в результате чего образуется пленка, называемая серебряное зеркало. Этот наблюдаемый результат очень красивый и используется в процессе производства промышленных зеркал.
Не останавливайся сейчас... После рекламы есть еще кое-что;)
Происходящую реакцию можно представить следующим образом:
О О
║ ║
R ─ C ─ H + H2О → R ─ C ─ OH + 2e- + 2 H+
2 Ag+ + 2e- → 2 Ag0
2 NH3 + 2 часа+ → 2 NH4+
О О
║║
R C ─ H + 2 Ag+ + 2 NH3 + H2О → R C ─ ОН + 2 Ag0 + 2 NH4+
альдегид Толленс реактивныйкарбоновая кислота серебристый металлик (серебряное зеркало)
С другой стороны, если мы заставим кетон реагировать с реактивным веществом Толленса, образования металлического серебра не произойдет, потому что кетоны не могут восстанавливать ионы Ag.+.
2- Реактив Фелинга: Этот реактив представляет собой синий раствор сульфата меди II (CuSO4) в основной среде, так как он смешивается с другим раствором, образованным гидроксидом натрия (NaOH) и тартратом натрия и калия (NaOOC-CHOH-CHOH-COOK). Тартрат добавляют к раствору сульфата меди II, чтобы стабилизировать его и предотвратить его осаждение.
CUSO4 + 2 NaOH → Na2ТОЛЬКО4 + Cu (OH)2
Реактивный Фелинг (названный в честь немецкого химика Германа фон Фелинга (1812-1885))
При контакте с реактивом Фелинга альдегид образует карбоновую кислоту путем ее окисления, а ионы меди (Cu)2+), присутствующие в середине, уменьшаются, образуя красновато-коричневый осадок (более похожий на кирпич), который представляет собой оксид меди. Кетоны, с другой стороны, не вступают в реакцию - потому что они не могут восстанавливать ионы Cu.2+.
О О
║ ║
R ─ C ─ H + 2 Cu (OH)2 → R ─ C ─ OH + Жопа2О + 2 часа2О
альдегид красновато-коричневый осадок
3- Реактив Бенедикта: Это реактивное вещество также образуется раствором сульфата меди II (Cu (OH)2) в основной среде, но он смешан с цитратом натрия.
Как и в случае с реактивом Фелинга, в случае реакции между альдегидом и реактивом Бенедикта также присутствуют ионы меди (Cu2+) присутствуют в среде, которые восстанавливаются и образуют красный оксид меди.
Этот реагент широко используется в тестах для определения наличия и содержания глюкозы в моче. Глюкоза имеет в своей структуре альдегидную группу, поэтому она вступает в реакцию с реагентом Бенедикта, присутствующим в полосках для этих тестов. Оттуда просто сравните цвет ленты с цветом шкалы на упаковке продукта.

Реагент Бенедикта используется для определения содержания глюкозы в моче.
Дженнифер Фогача
Окончила химический факультет
Хотели бы вы использовать этот текст в учебе или учебе? Посмотрите:
FOGAÇA, Дженнифер Роча Варгас. «Дифференциация альдегидов и кетонов»; Бразильская школа. Доступно в: https://brasilescola.uol.com.br/quimica/diferenciacao-aldeidos-cetonas.htm. Доступ 27 июня 2021 г.
Химия

Альдегиды, карбонильные соединения, карбонильная группа, основные альдегиды, этаналь, сырье в пестицидной и фармацевтической промышленности, метанал, формальдегид, пластмасса и полимерная промышленность.
Химия

Кетоны, органические вещества, карбонильная функциональная группа, получение растворителя эмали, пропанона, кетоновые тела в кровотоке, экстракция масел и жиров из семян растений, растворители Органический.