Acțiunea unui catalizator este în esență accelerarea dezvoltării unei anumite reacții. Acest lucru este posibil pentru că catalizatorul schimbă mecanismul prin care se desfășoară reacția, ducând la o „cale alternativă” care necesită mai puțină energie de activare pentru ca reacția să înceapă și să ajungă la complexul activat.
Există mai multe tipuri de cataliză, dintre care unul este cataliză eterogenă, care poate fi definit ca ceea ce apare atunci când sistemul are mai multe faze, adică reactanții și produsele sunt într-o stare fizică diferită de starea fizică a catalizatorului.
Un exemplu pe care îl putem menționa este un stadiu intermediar de formare a acidului sulfuric (H2NUMAI4 (aq)). Această etapă constă în formarea trioxidului de sulf (SO3 (g)) prin reacția de ardere a dioxidului de sulf (SO2 (g)):
2 ASA2 (g) + O2 (g) → 2 OS3 (g)
Deoarece această reacție se desfășoară atât de încet, se folosește un catalizator pentru a-l accelera. Un catalizator care poate fi utilizat în acest caz este pentanxidul de divanadiu (V
2O5 (S)), care este solid. Deoarece reactanții și produsul de reacție sunt gazoși, vom avea un sistem eterogen.Dar cum poate accelera reacția pentoxidul de divanadiu?
Ceea ce se întâmplă este că moleculele reactivului de oxigen sunt adsorbite, adică reținute pe suprafața pentoxidului de divanadiu. Acest lucru face ca legăturile moleculelor acestui gaz să se slăbească în timp, ceea ce facilitează formarea complexului activată și, în consecință, scade energia de activare a reacției, crescând viteza de dezvoltare a acesteia, adică a acesteia viteză.
Vedeți cum se întâmplă acest lucru în diagrama de mai jos:
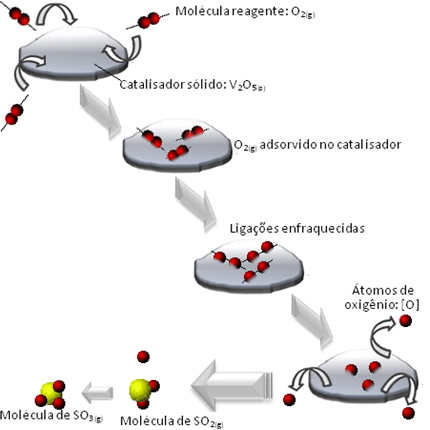
Alte exemple de cataliză eterogenă sunt prezentate mai jos. Rețineți că în ambele cazuri reactanții și produsele sunt în stare gazoasă, apoasă sau lichidă, în timp ce catalizatorii sunt în stare solidă:
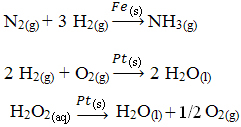
Un exemplu de cataliză eterogenă care apare în viața noastră de zi cu zi este cel al convertoarelor catalitic auto, mai bine cunoscut ca catalizatori. Aceste dispozitive anti-poluare sunt acoperite cu substanțe care acționează ca catalizatori, fiind de obicei un aliaj de paladiu și rodiu (pentru motoarele pe benzină) și paladiu și molibden (pentru motoarele pe benzină). alcool).
În cadrul acestui catalizator, apar reacții chimice în care gazele provenite din arderea incompletă, care sunt mai dăunătoare pentru oameni, sunt transformate în gaze netoxice. Reactanții și produsele sunt toate gaze, în timp ce catalizatorii sunt solizi.
Pentru a înțelege mai multe despre sistemul de operare al acestui echipament, citiți textul: "Convertor catalitic”.
De Jennifer Fogaça
Absolvent în chimie
Sursă: Școala din Brazilia - https://brasilescola.uol.com.br/quimica/catalise-heterogenea.htm
