Celulele sau celulele electrochimice și bateriile sunt dispozitive în care energia chimică este transformată spontan în energie electrică.Celula este formată din doar doi electrozi și un electrolit, în timp ce bateria este un set de baterii în serie sau în paralel.
La bateriile primare sunt dispozitive care nu se reîncarcă, fiind că atunci când reacția de oxidare-reducere care are loc în interiorul lor încetează, acestea trebuie aruncate.
Pentru fiecare echipament, este indicat un tip de baterie și, printre bateriile principale utilizate în prezent, principalele sunt: Celule uscate Leclanché (baterii comune sau celule acide), baterii alcaline și baterii cu dioxid de litiu / mangan.
Vedeți ce le face diferite și pentru ce echipamente sunt potrivite:
- Celule uscate Leclanché:
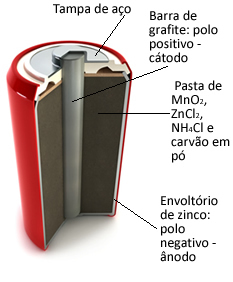
Aceste grămezi sunt formate practic dintr-un plic de zinc, separat de o hârtie poroasă și de o bară centrală de grafit înconjurată de dioxid de mangan (MnO2), cărbune praf (C) și o pastă umedă conținând clorură de amoniu (NH4Cl), clorură de zinc (ZnCl2) și apă (H2O).
O zinc funcționează ca anod, pierderea electronilor; este grafit funcționează ca catod, conducerea electronilor către dioxidul de mangan:
Jumătate de reacție anodică: Zn (s) → Zn2+(Aici) + 2 și-
Semi-reacție catodică: 2 MnO2 (aq) + 2 NH41+(Aici) + 2e- → 1 Mn2O3(s) + 2NH3 (g) + 1 oră2O(1)
Reacție globală: Zn (s) + 2 MnO2 (aq) + 2 NH41+(Aici) → Zn2+(Aici) + 1 Mn2O3 (e) + 2NH3 (g)
Acest tip de baterie este potrivit pentru echipamente care necesită descărcare ușoară și continuă, cum ar fi telecomandă, ceas de perete, radio portabil și jucării.
Puteți obține mai multe detalii despre origine, funcționare, durabilitate, ddp, pericole și precauții care trebuie luate cu aceste baterii în textul „Leclanché Dry Stack”.
Nu te opri acum... Există mai multe după publicitate;)
- Baterii alcaline:
Funcționarea sa este foarte asemănătoare cu cea a celulelor uscate Leclanché, cu toate acestea, singura diferență este aceea în locul clorurii amoniu (care este o sare acidă), se adaugă o bază puternică, în principal hidroxid de sodiu (NaOH) sau hidroxid de potasiu (KOH).
Jumătate de reacție anodică: Zn + 2 OH → ZnO + H2O + 2e-
Semi-reacție catodică: 2 MnO2 + H2O + 2e-→ Mn2O3 + 2 OH
Reacție generală: Zn +2 MnO2→ ZnO + Mn 2O3

Bateriile alcaline sunt mai avantajoase decât cele acide în sensul că au o durabilitate mai mare, în furnizează de obicei cu 50-100% mai multă energie decât o baterie obișnuită de aceeași dimensiune, plus că există un pericol mai mic scurgeri.
Acestea sunt indicate în principal pentru dispozitivele care necesită descărcări rapide și mai intense, cum ar fi aparate de radio, CD / DVD portabile și playere MP3, lanterne, camere digitale etc.
Citește și textul Baterii alcaline.
- Baterii litiu / dioxid de mangan:
Aceste baterii sunt ușoare și generează o tensiune mare (aproximativ 3,4 V), motiv pentru care sunt adesea utilizate în echipamente mici, cum ar fi ceasurile și calculatoarele. Spre deosebire de cazurile anterioare, formatul său este moneda, așa cum se arată în următoarea imagine:

Anodul este litiu, catodul este dioxid de mangan și electrolitul este o soluție salină:
Jumătate de reacție anodică: citit →citit+ + și−
Semi-reacție catodică: MnO2 + citit+ + și−→MnO2(li)
Reacție generală: Li + MnO2 → MnO2(li)
De Jennifer Fogaça
Absolvent în chimie
Doriți să faceți referire la acest text într-o școală sau într-o lucrare academică? Uite:
FOGAÇA, Jennifer Rocha Vargas. „Cele mai frecvente tipuri de celule și baterii primare”; Școala din Brazilia. Disponibil in: https://brasilescola.uol.com.br/quimica/tipos-pilhas-baterias-primarias-mais-comuns.htm. Accesat la 27 iunie 2021.

