Tu metale sunt elemente chimice care au ca principală caracteristică fizică capacitatea de a pierde electroni și, în consecință, formează cationi metalici. Din acest motiv, pot face două tipuri de legături chimice: legătura ionică și legătura legătură metalică.
THE legătură ionică apare atunci când un metal interacționează cu un element de natură metalică, care poate fi un ametal sau hidrogen. În acest tip de legătură, avem pierderea de electroni de către metale și câștigul de electroni de către nemetale sau hidrogen.
deja legătură metalică se stabilește între atomii unui singur element metalic. Acest tip de legătură apare numai între atomii unui singur metal și exclusiv deoarece un metal nu poate stabili o legătură chimică cu un alt element metalic diferit.
Caracteristicile generale ale metalelor
Solidele la temperatura camerei, cu excepția mercurului;
Sunt geniali;
Au puncte de topire și fierbere ridicate;
Ele sunt în general de culoare argintie, cu excepția aurului, care este auriu, și a cuprului, care este roșiatic;
Metalele pure sunt formate din grupuri de atomi (dintr-un singur element chimic) numite rețele cristaline.
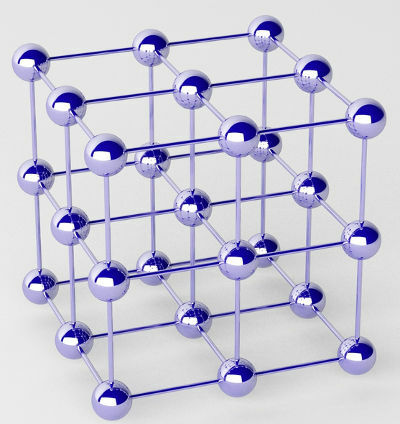
Reprezentarea rețelei cristaline a unui metal
Principiile lipirii metalice
La legătură metalică, rețelele cristaline care formează metalele sunt de fapt un cluster ionic (compus doar din cationii și electroni). Electronii prezenți în stratul de valență al atomilor metalici sunt delocalizați, adică părăsesc stratul de valență, determinând atomul să devină un cation (deficitar în electroni).
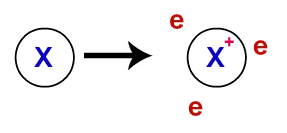
Reprezentarea electronilor delocalizați din coaja de valență
După ce sunt delocalizați, electronii din atomii metalici încep să înconjoare cationii, formând o adevărată „mare de electroni”. Fiecare dintre electronii prezenți în această mare are capacitatea de a se deplasa liber prin rețeaua cristalină a metalului.

Reprezentarea modelului mării electronilor
NOTĂ: Electronii „din mare” nu sunt capabili să părăsească rețeaua de cristal și să se miște prin ea.
Proprietățile metalelor justificate prin lipirea metalică
a) Maleabilitatea
Prin intermediul unui metal, este posibil să se producă foi de diferite grosimi și foi. Datorită acestei proprietăți a metalelor putem construi diverse obiecte, precum cuțite, săbii etc.

Lama unei sabii este realizată dintr-un metal
b) Conductivitate
Metalele, în general, sunt bune conductoare ale curentului electric și ale căldurii. Când orice metal este în contact cu o sursă de căldură sau o sursă de curent electric, este capabil să le conducă.

O tigaie de aluminiu în flacăra unei sobe devine complet fierbinte datorită conductivității.
c) Ductibilitate
Prin intermediul unui metal, putem produce fire. Utilizarea unui metal sub formă de fire facilitează utilizarea acestuia, în special în ceea ce privește conductivitatea electrică.

Un metal, cum ar fi cuprul, poate fi folosit pentru a produce fire.
De mine. Diogo Lopes Dias
Sursă: Școala din Brazilia - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-ligacao-metalica.htm
