În laboratoare și în industria chimică este foarte important să se cunoască cantitatea de substanțe implicate în reacții. Prin urmare, mai jos vom trata principalele concepte, mărimi și unități de măsură legate de masele atomilor:
- Unitatea de masă atomică (u):
Atomul de referință al greutății standard pentru a desemna unitatea de masă atomică este carbon-12 (12Ç). O unitate de masă atomică (1 u) corespunde valorii de 1.66054. 10-24 g, care este masa de 1/12 a izotopului de carbon cu o masă egală cu 12 (12Ç).
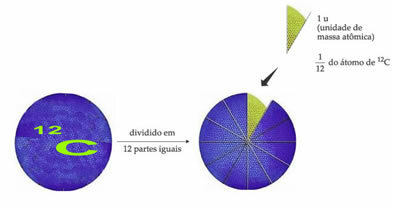
Unitatea de masă atomică (u) este unitatea utilizată în toate cantitățile enumerate mai jos.
- Masa atomică a unui atom sau izotop (MA):
Se obține comparându-l cu valoarea de referință menționată în articolul anterior. De exemplu, masa atomică a 919F este dat de spectrometrul de masă, care este egal cu 18,9984 u. Rotunjind în sus, este egal cu 19, care este aceeași valoare cu numărul său de masă (A). Această valoare înseamnă că masa atomică a elementului 919F este de 19 ori mai mare decât masa de 1/12 din 12Ç.
- Masa atomică a unui element (AM):
Masa atomică a elementului este determinată de media ponderată a maselor atomice ale izotopilor săi. Acest lucru se face prin înmulțirea maselor atomice ale fiecărui izotop cu procentul care apare în constituția elementului. Aceste valori sunt apoi adunate, care sunt împărțite la 100, rezultând procentul total.
De exemplu, elementul neon este compus din trei izotopi cu următoarele mase atomice și procente în constituția lor:

Calculând masa atomică (MA) a acestui element:
RĂUneon = (20. 90,92) + (21. 0,26) + (22. 8,82)
100
RĂUneon = 20.179 u
- Masa moleculară (MM):
După cum sugerează și numele, este folosit pentru substanțe moleculare, adică atomi legați printr-o împărțire a perechilor de electroni, care sunt numite legături covalente.
Masa moleculară se obține înmulțind numărul de atomi ai fiecărui element cu masele lor atomice și adăugând rezultatele.
De exemplu, molecula de CO2 conține un carbon și doi oxigeni, deci vom înmulți masa atomică a carbonului cu 1; și oxigenul la două, adăugându-le mai târziu:
MMCO2 = (1. RĂUÇ) + (2. RĂUO)
MMCO2 = (1. 12) + (2. 16)
MMCO2 = 12 + 32
MMCO2 = 44 u
- Formula de masă:
Totuși, este același calcul efectuat pentru masa moleculară pentru compușii ionici. În acest caz, numele este diferit, deoarece acestea nu sunt grupate în molecule, ci în grupuri de ioni. Deoarece moleculele nu există, în mod evident nu are sens să vorbim despre masa moleculară, dar raționamentul din spatele calculului este același.
Exemplu:
NaCI
↓ ↓
23 +35,5 → Masa formulei = 58,5 u
De Jennifer Fogaça
Absolvent în chimie
Sursă: Școala din Brazilia - https://brasilescola.uol.com.br/quimica/massas-dos-atomos.htm
