Combustibilii folosiți în majoritatea mașinilor sunt benzina și etanolul. Arderea completă a acestor doi combustibili generează dioxid de carbon (CO2 (g)) și apă (H2O). Din păcate, însă, arderea incompletă și impuritățile prezente în alcool și benzină pot genera substanțe foarte poluante pentru mediu. În cazul benzinei, monoxidul de carbon (CO(g)); hidrocarburi (compuși constând din carbon și hidrogen), cum ar fi etanul (C2H6 (g)); și oxizi de azot (NOX), în principal monoxid de azot (NO) și dioxid de azot (NO2 (g)).
Astfel, pentru a evita o creștere a poluării aerului, toate mașinile au nevoie de echipamente numite convertorul catalitic sau convertorul catalitic, care este un dispozitiv anti-poluare, care are funcția de a trata aceste gaze degajate de motorul cu ardere internă și de a le transforma în gaze mai puțin dăunătoare. Convertorii catalitici sunt de asemenea utilizați în acest scop în unele procese industriale.
Gazele poluante menționate părăsesc motorul și intră în convertorul catalitic, trecând printr-un fel de „stup”, ale căror celule sunt în general fabricate din material ceramic sau metalic, care este acoperit cu alumină (oxid de aluminiu - Al
2O3). Această formă de fagure de miere, cu canale minuscule, este importantă deoarece oferă o suprafață mare de contact pentru gaze, făcându-le să reacționeze mai rapid.Dar adevăratul catalizator este un metal care se află deasupra oxidului de aluminiu. De obicei, metalele utilizate sunt paladiu, rodiu, platină sau molibden. De asemenea, puteți amesteca aceste metale și puteți folosi aliaje. De exemplu, în cazul benzinei, se folosește în mod normal un aliaj de paladiu și toriu; în cazul etanolului, se utilizează un alt aliaj de paladiu și molibden. Aceste metale efectuează o cataliză eterogenă cu gaze poluante.
cataliză eterogenă este un tip de reacție în care catalizatorul formează cu reactanții (în acest caz, gazele poluante) un sistem polifazic. Acest lucru se datorează faptului că catalizatorul se adsorbe, adică reține moleculele reactanților pe suprafața sa, slăbindu-le legăturile și făcând reacția să se desfășoare mai rapid.
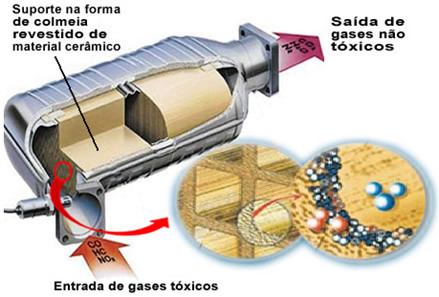
Ca rezultat, metalele catalizatoare transformă agenți poluanți precum CO și NOX în gaze netoxice precum CO2, H2O, O2 si nu2. Vedeți câteva dintre aceste reacții mai jos și observați că prin ele există oxidarea hidrocarburilor și CO (derivat din arderea incompletă) și, de asemenea, reducerea oxizilor de azot la azot gazos (N2):
2 CO(g) + 2 NU(g) → 2 CO2 (g) + 1 N2 (g)
2 CO(g) + 1 O2 (g) → 2 CO2 (g)
2C2H6 (g) + 7 O2 (g) → 4 CO2 (g) + 6 H2O(v)
2 NU2 (g) +4 CO(g) → 1 N2 (g) + 4 CO2 (g)
2 NU2 (g) → 1 N2 (g) + 2 O2 (g)
2 NU(g) → 1 N2 (g) + 1 O2 (g)
De Jennifer Fogaça
Absolvent în chimie
Sursă: Școala din Brazilia - https://brasilescola.uol.com.br/quimica/conversor-catalitico.htm
