Una dintre caracteristicile principale care disting o reacție de oxidare-reducere (sau redox) dintre celelalte este prezența unui agent oxidant și a unui agent reducător, care poate fi definit după cum urmează:
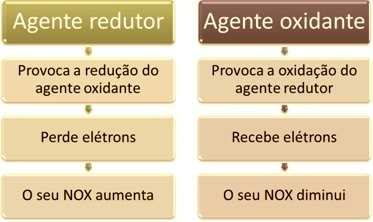
De exemplu, priviți reacția chimică de mai jos, unde aluminiu (Al) se corodează în soluție apoasă de acid clorhidric (HCI). Atomii de aluminiu transferă electronii către cationii H.+(Aici) și produce cationul Al3+(Aici):
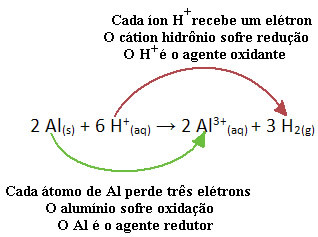
Rețineți că, din moment ce Al a transferat electroni, aceasta înseamnă că a provocat reducerea a cationilor H+(Aici); de aceea este chemat agent de reducere. Deja cationul H+(Aici) a scos electronii din aluminiu, provocând oxidare din acel metal; de aceea acționează ca un agent oxidant.
În viața de zi cu zi, există multe exemple de performanță a agenților oxidanți și a agenților reducători. Uitați-vă la unele dintre ele și amintiți-vă, totuși, că în toate cazurile reducerea are loc simultan cu oxidarea; prin urmare, dacă există un agent reducător, există și un agent oxidant.
- Exemple de agenți reducători:
- În filmele fotografice: filmele fotografice conțin săruri de argint sensibile la lumină. În punctele în care există incidența luminii, există o reducere a ionilor Ag+, rezultând contrastul observat la negative.

- Vitamina C: Vitamina C (acidul L-ascorbic) este un agent de reducere puternic în soluție apoasă. Are o facilitate excepțională pentru a fi oxidat și de aceea este utilizat pe scară largă, în special în alimente precum a antioxidant, adică se adaugă la alte alimente și le protejează de o posibilă oxidare, datorită propriei sale sacrificiu. Un exemplu îl reprezintă fructele precum merele și perele care se întunecă în contact cu oxigenul din aer, deoarece se oxidează. Dar când adăugați o cantitate mică de suc de portocale sau lămâie (care conțin vitamina C) la fructe tăiat, acest lucru împiedică apariția acestei reacții, deoarece vitamina C acționează ca un agent reducător și se oxidează înaintea fructului.

- Hidrogen gazos: hidrogenul gazos (H2) este utilizat în propulsia cu rachete și este considerat una dintre cele mai importante alternative energetice, deoarece arderea acestuia eliberează o cantitate mare de energie și nu prezintă poluanți. În această reacție, hidrogenul acționează ca un agent reducător, fiind oxidat de oxigen.
- Exemple de agenți oxidanți:
- În producția de oțet: când vinul este expus aerului, acesta se transformă în oțet, a cărui componentă principală este acidul acetic. Acest lucru se datorează faptului că alcoolul etilic sau etanolul prezent în vin se oxidează la contactul cu oxigenul atmosferic, rezultând acid acetic. Astfel, oxigenul este un agent oxidant. Chiar și originea termenului „oxidare” este legată de reacția cu oxigenul.

- În rugină: după cum sa menționat în exemplul anterior, oxigenul acționează ca agent oxidant pentru alcool; și face acest lucru și în contact cu diferite metale, cum ar fi fierul, provocând procesul de ruginire. Pe lângă oxigenul din aer, alți agenți de oxidare în acest caz sunt apa sau o soluție acidă.
- În înălbitori: efectul de înălbire al înălbitorilor se datorează prezenței următorilor doi agenți reducători: o anion hipoclorit (în general sub formă de sare de sodiu - NaOCl), prezent, de exemplu, în înălbitor; și peroxid de hidrogen (H2O2), comercializat sub formă de peroxid de hidrogen. Acești doi compuși au o tendință foarte puternică de oxidare și determină reducerea altor specii chimice. Prin urmare, acestea sunt responsabile de substanțele oxidante care conferă produse întunecate. De exemplu, în celuloză, lignina se descompune și devine mai ușoară și mai maleabilă. În cazul îndepărtării petelor și înălbirii țesăturilor, acești agenți oxidanți determină oxidarea moleculelor organice, cum ar fi grăsimile și coloranții.

- În etiloteste: un etilotest simplu de unică folosință constă dintr-un tub transparent care conține o soluție apoasă de sare dicromat de potasiu și silice, umezită cu acid sulfuric; amestecat cu culoarea portocalie. Această sare, în contact cu vaporii de alcool conținuți în respirația șoferului beat, reacționează, schimbând culoarea în verde. Aceasta înseamnă că este cauzată oxidarea etanolului (alcoolului) la etanal.

De Jennifer Fogaça
Absolvent în chimie
Sursă: Școala din Brazilia - https://brasilescola.uol.com.br/quimica/conceito-exemplos-agente-redutor-agente-oxidante.htm
