THE nihonium, numar atomic 113 și simbolul Nh, este un element chimic aparținând grupei 13 din Tabelul Periodic. În plus, este un element supergreu care nu se găsește în natură. Astfel, obținerea lui se poate face doar artificial, prin reacții de fuziune nucleară. Caracteristicile chimice ale nihoniului sunt încă neclare, dar se speculează că acesta se comportă similar cu omologul său mai ușor, taliul, în unele cazuri.
Nihonium a fost obținut inițial prin topire 70Zn cu 209Bi, la Institutul Riken, Japonia, în 2003. Deși oamenii de știință ruși și americani au cerut să fie recunoscuți ca descoperitori ai elementului 113, IUPAC i-a recunoscut pe oamenii de știință japonezi. Numele se referă la cuvântul Nihon, așa cum își numesc japonezii țara natală.
Citeste si: Galiu - un alt element chimic aparținând grupei 13 din Tabelul Periodic
Subiecte din acest articol
- 1 - Rezumat despre nihonium
- 2 - Proprietățile nihoniului
- 3 - Caracteristicile nihonium
- 4 - Obținerea nihoniumului
- 5 - Istoria lui Nihônio
- 6 - Exerciții rezolvate pe nihonium
rezumat despre nihonium
Este un element chimic sintetic situat în grupul 13 al Tabelul periodic.
Producția sa a început în 2003, la Institutul Riken, Japonia.
El alcătuiește grupul de elemente cel mai recent inclus în Tabelul Periodic, în 2015.
Studiile sale sunt încă foarte recente, dar unii încearcă să o lege de alte elemente din grupa 13, precum taliul.
Producția sa este Fuziune nucleară, folosind izotopi ai 70Zn și atomi de 209Bi.
Nu te opri acum... Mai sunt dupa anunt ;)
Proprietățile nihonium
Simbol: nah
Numar atomic: 113
Masă atomică: intre 278 si 286 c.u. (neoficial de Iupac)
Configuratie electronica: [Rn] 7s2 5f14 6d10 7p1
Cel mai stabil izotop:286Nh (9,5 secunde de jumătate de viață, care poate crește cu 6,3 secunde sau poate scădea cu 2,7 secunde)
Seria chimică: grupa 13, elemente super grele
caracteristicile nihoniului
Nihonium, simbolul Nh și numărul atomic 113, a fost unul dintre ultimele elemente incluse în Tabelul Periodic. Oficializarea sa a avut loc la 30 decembrie 2015, de către Uniunea Internațională de Chimie Pură și Aplicată (IUPAC), în timp ce numele său a fost oficializat abia la jumătatea anului 2016.
Elementele din această regiune a tabelului periodic sunt extrem de instabile, ceea ce înseamnă că nu pot fi găsite în natură. Astfel, în fața unei presupuse existențe, ele ar suferi dezintegrare radioactivă aproape instantaneu - emisia de particule nucleare, precum α și β - pentru a obține o mai mare stabilitate.
Cu toate acestea, atunci când emit particule nucleare, ajung să sufere o transmutare nucleară, adică devin un nou element chimic. Astfel, elementele supergrele, precum Nh, trebuie produse în laborator, ceea ce îl face a element chimic sintetic.
Nh, ca și alte elemente supergrele, este influențat de efecte relativiste — într-un mod simplu, distanțe de la ceea ce se observă la ceea ce se aștepta, datorită relativității. Astfel, studiile matematice din domeniul teoretic, care simulează consecințele efectului relativist, au evidențiat că nihonium ar putea interacționa slab cu cuarțul, dar a avea buna adsorbtie la aur, ca omologul său mai ușor, taliul (Tl).
Studiile teoretice preliminare au indicat de asemenea volatilitate din Nh. În ceea ce privește adsorbția la cuarț, taliul formează ușor TlOH, de exemplu, și se suspectează că nihoniul face același lucru.
Chiar și așa, cum studiile sunt încă foarte preliminare și recente, mare parte din ceea ce a fost produs este deschisă discuțiilor și este dificil să se determine cu exactitate proprietățile fizico-chimice ale nihoniului.
Obținerea Nihoniumului
Elementul 113, până astăzi, a fost obținut în două moduri: prin reacții de fuziune la rece, cu fuziunea zincului (Zn, Z = 30) cu bismut (Bi, Z = 83), precum și prin dezintegrarea alfa a elementului 115.
În primul exemplu, zinc este accelerată la 10% din viteza luminii, pentru a depăși forțele de respingere ale celor două nuclee. Apoi se produce un izotop 279Nh, care ajunge să emită un neutron și să producă 278Nh.

Cu un timp de înjumătățire de aproximativ 34 de milisecunde, izotopul 278Nh suferă șase descompunere alfa (emisii de particule alfa) la elementul mendeleviu (Md).
În al doilea caz, elementul 113 ia naștere din dezintegrarea alfa a elementului 115 (cunoscut acum ca muscovium) după ce a fost sintetizat. O modalitate este reacția de fuziune la cald a ionilor 48Ca cu izotopi 243ah, producând 288Mc și apoi, prin dezintegrare alfa, the 284Nh, care continuă să sufere dezintegrare alfa.
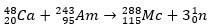
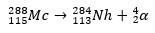
Vezi si: Hassium - cel mai greu element chimic sintetic care are proprietățile analizate
istoria nihoniumului
Căutările pentru elementul 113 au început în 2003. Cercetătorii japonezi de la Institutul Riken au accelerat izotopii 70Zn la 10% din viteza luminii pentru a se ciocni cu 209Bi, printr-o reacție de fuziune. Astfel, au reușit să producă ceea ce știm acum ca 278Nh.
Cu toate acestea, abia în 2012 Cercetătorii japonezi au reușit să detecteze seria completă de dezintegrare alfa a elementului 113, contactând IUPAC pentru a revendica descoperirea.
Concomitent cu eforturile japoneze, oamenii de știință ruși conduși de Yuri Oganessian, în colaborare cu Oamenii de știință americani au ajuns, de asemenea, să identifice elementul 113 prin descompunerea alfa a elementului 115. Astfel de experimente i-au pus pe oamenii de știință ruși și americani în competiție pentru recunoașterea elementului 113.

Cu toate acestea, IUPAC a constatat că dovezile de la institutul Riken sunt mai solide și, astfel, a permis japonezilor să aibă dreptul de a numi elementul 113. Numele ales a fost nihônio, simbolul Nh, cu referire la țară Japonia. Cuvântul Japonia este scris de japonezi folosind două caractere chinezești care înseamnă „țara soarelui răsărit” și sunt citite ca Nihon sau Nippon.
Numele de nihonium a fost ales și pentru că, în 1908, chimistul japonez Masataka Ogawa a publicat că descoperise elementul 43, numindu-l japoneză, simbol Np (care astăzi aparține neptuniului, Z = 93). Totuși, ulterior, s-a dovedit că elementul 43 era instabil, nefiind găsit în natură și a fost sintetizat abia în 1937, primind denumirea de tehnețiu (Tc).
Astfel, japoneza a dispărut din Tabelul Periodic. Cu toate acestea, ani mai târziu, s-a dovedit că, de fapt, Ogawa descoperise elementul 75 (cunoscut acum ca reniu). Cu toate acestea, până la acel moment, elementul reniu fusese deja descoperit oficial în 1925 și botezat.
Exerciții rezolvate pe nihonium
intrebarea 1
Nihonium, simbolul Nh și numărul atomic 113, este un element chimic care nu poate fi găsit în natură din cauza timpului său scurt de înjumătățire. Cel mai rezistent dintre ei, cel 286Nh, are aproximativ 9,5 secunde. Știind că timpul de înjumătățire este timpul necesar pentru ca cantitatea de specii să scadă la jumătate, câte secunde durează pentru ca cantitatea de izotop de mai sus să fie 1/16 din cantitate iniţială?
A) 9.5
B) 19
C) 28,5
D) 38
E) 47,5
Rezoluţie:
Alternativa D
La fiecare 9,5 secunde, cantitatea de izotop scade la jumătate. Deci, după 9,5 secunde, cantitatea sa este jumătate din cantitatea inițială. Încă 9,5 secunde, însumând 19 secunde, cantitatea scade din nou la jumătate, ajungând la 1/4 din inițială.
La 28,5 secunde, după un alt timp de înjumătățire, cantitatea scade din nou la jumătate, ajungând la 1/8 din cantitatea inițială. În cele din urmă, după 38 de secunde, suma scade din nou la jumătate, ajungând la 1/16 din suma inițială, așa cum se solicită în extras. Astfel, timpul necesar este de 38 de secunde.
intrebarea 2
În 2003, căutarea elementului 113 a început la Institutul Riken din Japonia. La acel moment, oamenii de știință au fost capabili să producă 278Nh prin fuziunea atomilor de zinc și bismut.
Câți neutroni sunt în izotopul citat?
A) 113
B) 278
C) 391
D) 170
E) 165
Rezoluţie:
Alternativa E
Numarul neutroni poate fi calculat ca:
A = Z + n
unde A este numărul de Paste atomic, Z este numărul atomic și n este numărul de neutroni. Înlocuind valorile, avem:
278 = 113 + n
n = 278 - 113
n = 165
De Stefano Araújo Novais
Profesor de chimie
