THE oganesson, simbolul Og, numar atomic 118, este elementul chimic cu cel mai mare număr atomic din Tabelul Periodic de până acum. Nu se găsește în natură, iar producția sa este artificială, deci este considerat un element sintetic. Chiar și așa, producția sa este foarte dificilă și este considerat un element foarte rar, fiind sintetizat de foarte puține ori.
În ciuda faptului că se află în același grup cu cei gaze nobile, oganessonul nu are multe caracteristici care să se refere la aceste elemente, conform calculelor matematicienii demonstrează, ca o consecință a efectelor relativiste pe care le suferă elementele supragrele.
Elementul 118 a fost sintetizat pentru prima dată în 2002, prin reacția ionilor 48Ca cu atomi de 249Vedea Numele său este un omagiu adus savantului rus Yuri Oganessian, unul dintre cele mai respectate și recunoscute în zona elementelor supergrele.
Vezi si: Rutherfordium - elementul chimic sintetic numit după omul de știință Ernest Rutherford
Rezumat despre oganesson
Oganesona este un element chimic sintetic situat în grupul 18 al Tabelul periodic.
A fost sintetizat pentru prima dată în 2002, într-o lucrare comună între oamenii de știință ruși și americani.
El alcătuiește grupul de elemente cel mai recent inclus în Tabelul Periodic, în 2016.
Este un element foarte rar, fiind sintetizat de foarte puține ori.
Studiile lor sunt încă foarte recente, proprietățile de bază fiind încă determinate de calcule și modele matematice.
Testele teoretice preliminare indică faptul că, deși aparțin grupului de gaze nobile, unele proprietăți distanță Og de celelalte elemente.
Producerea de oganesone are loc prin Fuziune nucleară, folosind ioni de 48Ca și atomi de 249Vedea
Numele său este un omagiu adus savantului rus Yuri Oganessian, unul dintre cei mai importanți în domeniul studiului elementelor supergrele.
Nu te opri acum... Mai sunt dupa anunt ;)
proprietățile oganesson
Simbol: Oh
Numar atomic: 118.
Masă atomică: 294 c.u. (neoficial de Iupac).
Configuratie electronica: [Rn] 7s2 5f14 6d10 7p6.
Cel mai stabil izotop: 294Og (timp de înjumătățire de 0,69 milisecunde, care poate fi mărit cu 0,64 milisecunde sau redus cu 0,22 milisecunde).
Seria chimică: grupa 18, elemente supergrele, gaze nobile.
Caracteristicile lui oganesson
Oganesson este elementul cu cel mai mare număr atomic (118) oficializat până acum de către Uniunea Internațională de Chimie Pură și Aplicată (IUPAC). Deși a fost produs pentru prima dată în 2002, se stie putine despre el. Se speculează încă multe, deoarece acest element nu se găsește în natură. Producția sa se realizează în laborator, care îl configurează ca element sintetic.
În plus, ta jumătate de viață este mai mică de o milisecundă (10-3 al doilea) — amintindu-ne că timpul de înjumătățire este timpul necesar pentru ca cantitatea să se înjumătățește. Prin urmare, proprietățile care sunt stipulate pentru acest element nu sunt altceva decât rezultatele calcule teoretice bazate pe modele matematice, deoarece în regiunea Tabelului periodic în care se află găsește efecte relativiste (discrepanța dintre efectele așteptate și cele observate ca urmare a relativității) sunt semnificative.
Efectele relativiste îl îndepărtează pe Og de ceea ce se aștepta de la el. Elementul, de exemplu, nu are un comportament similar cu gazele nobile. Calculele arată că oganesona ar fi un solid la temperatura camerei, cu un punct de topire în intervalul de 325 ± 15 K (aproximativ 52 °C) și un punct de fierbere în intervalul de 450 ± 10 K (aproximativ 177 °C).
De asemenea, se știe că Og poate fi mai reactiv decât alte gaze nobile, deoarece efectele relativiste îi permit să piardă mai ușor electronii de subnivelul p. Un alt punct de dezacord cu gazele nobile este că oganesone este a semiconductor, în timp ce celelalte sunt izolatoare.
Citeste si: Hidrogen - elementul chimic care are cel mai mic număr atomic din Tabelul Periodic
Obținerea oganesson
Ca și alte elemente supergrele, oganesson este obținut printr-o tehnică numită topitură la cald, unde ionii izotopului 48Ca, găsit în mod natural, dar foarte puțin disponibil, reacționează cu izotopi mult mai grei pentru a produce elemente supergrele.
Og este un element atât de rar și greu de obținut încât într-un interval de zece ani, doar patru atomi a ajuns să fie produs. Practic, producția de 294Og, singurul izotop cunoscut, apare prin bombardarea ionică 48Ca la un miez de 249Cf, cu eliberare a 3 neutroni.
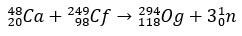
Cu câteva milisecunde de timp de înjumătățire, Og a fost identificat prin modelul său de dezintegrare, ceva foarte comun pentru elementele super-grele. În acest caz, s-au produs 3 descompunere alfa, determinând elementul 118 să devină coperniciu, Cn, care, în cele din urmă, a suferit fisiune spontană.
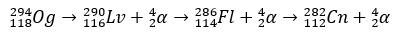
istoria lui Oganesson
Prima sinteză a oganessonului a avut loc în 2002., în orașul Livermore, California, Statele Unite, la Laboratorul Național Lawrence Livermore, unde un grup de oameni de știință americani a colaborat cu cercetători ruși al celebrului Institut Comun pentru Cercetare Nucleară (JINR), condus de omul de știință rus Yuri Oganessian.
Într-o perioadă de zece ani de la prima sinteză au fost sintetizați doar patru atomi de oganesonă, din cauza rarității și dificultății parametrilor de reacție. Cel de-al patrulea și ultimul atom, însă, a prezentat o descoperire incredibilă.
Oamenii de știință încercau să sintetizeze elementul 117 prin reacția lui 48Ca cu 249Bk, cu toate acestea s-a observat că 28% din ținta de berkeliu a suferit o dezintegrare β, transformându-se în 249Cf și astfel elementul generator 118. Este de remarcat faptul că numele elementului 118 îl onorează pe savantul rus Yuri Oganessian, un tribut care pentru chimiștii vii a avut loc doar de două ori în istoria chimiei, primul fiind pentru Glenn Seaborg, cu seaborgiu.
Exerciții rezolvate pe oganesson
intrebarea 1
Oganessona, element cu număr atomic 118 și simbolul Og, a fost plasat în perioada a șaptea a Tabelului Periodic, în grupa gazelor nobile. Ca urmare, s-au speculat mult dacă un astfel de element ar prezenta o mare stabilitate, o caracteristică cunoscută celorlalte elemente ale acestui grup. Alocarea lui Og în grupa 18 s-a datorat:
A) acest element este foarte stabil.
B) acest element are opt electroni în învelișul său de valență.
C) acest element este în mod demonstrabil un gaz la temperatura camerei.
D) acest element are aceleași proprietăți chimice ca și celelalte gaze nobile.
E) acest element are o energie de ionizare mare.
Rezoluţie:
Alternativa B
Alocarea Og-ului are loc numai și exclusiv pe seama acestuia distributie electronica. Faptul că are opt electroni înăuntru strat de valență, 7s2 7p6, îl pune în acea poziție. Studiile cu acest element sunt încă preliminare, dar deja se speculează, datorită rezultatelor matematice, că Og nu este un gaz la temperatura camerei, de exemplu. Un alt punct de subliniat este că Og nu este deloc stabil, nici măcar nu există în natură.
intrebarea 2
Marea dificultate în producerea elementului 118 generează ideea că oamenii de știință se aflau într-o adevărată odisee pentru a-l putea detecta. Nu e de mirare, după zece ani de la prima sa sinteză, oganesson a fost sintetizat doar de alte trei ori. Și până acum, se cunoaște un singur izotop, cel 294Oh Câți neutroni are izotopul cunoscut al lui Oganesson?
A) 294.
B) 118.
C) 176.
D) 412.
E) 166.
Rezoluţie:
Alternativa C
Numarul neutroni de Og poate fi calculat după cum urmează:
A = Z + n
A este numărul de Paste atomic, Z este numărul de protoni (sau numărul atomic) și n este numărul de neutroni. Înlocuind valorile, avem:
294 = 118 + n
n = 294 - 118
n = 176
De Stefano Araújo Novais
Profesor de chimie

