Cu cât temperatura este mai mare, cu atât este mai mare viteza unei reacții.
Acest lucru poate fi observat cu ușurință în multe situații din viața noastră de zi cu zi, ca în următoarele exemple:
- Când vrem să încetinim reacția de descompunere a unui aliment, scădem temperatura, punând-o în frigider;

- Dacă vrem să accelerăm reacția de gătit a alimentelor, puneți-o într-o oală de gătit. presiune care, odată cu creșterea presiunii, crește și temperatura de fierbere a apei lichide în care mancarea este;

- Incendiile, în general, sunt de obicei devastatoare, deoarece temperatura mediului crește, ceea ce determină o creștere a vitezei reacției de ardere;
- Pentru a încetini procesele chimice metabolice, scăzând șansele de afectare a creierului datorate deficit de oxigen, unele intervenții chirurgicale se efectuează prin scăderea temperaturii corpului pacientului, ajungând în jur 15 ° C;
- Dacă punem o tabletă efervescentă într-un pahar cu apă fierbinte și alta într-un pahar cu apă rece, prima se va dizolva mult mai repede.
Dar ce explică influența direct proporțională a temperaturii asupra vitezei de reacție?
Acest lucru se datorează faptului că, așa cum este explicat în text „Condiții pentru apariția reacțiilor chimice”, Pentru ca o reacție să poată continua, este necesar să îndeplinim anumite condiții, cum ar fi ca particulele trebuie să se ciocnească eficient și cu energia minimă necesară, care se numește energie de activare.
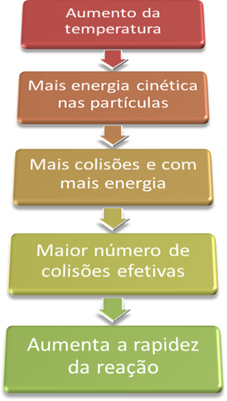
Astfel, atunci când creștem temperatura sistemului, creștem și agitația particulelor care reacționează și le oferim mai multă energie cinetică. Cu aceasta, vor apărea mai multe coliziuni și cu mai multă energie, crescând cantitatea de particule care vor reacționa și, în consecință, mărind viteza de reacție.
De Jennifer Fogaça
Absolvent în chimie
Sursă: Școala din Brazilia - https://brasilescola.uol.com.br/quimica/temperatura-velocidade-das-reacoes.htm

