se numește Modelul Rutherford propunerea atomului făcută de omul de știință Ernest Rutherford în 1911, cu scopul de a demonstra forma și compoziția idealizate a constituentului materiei: atom.
O Modelul Rutherford este cunoscut în mod obișnuit ca modelul sistemului solar, deoarece structura și funcționarea sa au fost comparate cu relația dintre soare și planetele care se învârt în jurul lui.
În modelul său, Rutherford a comparat soarele cu nucleul atomului, iar electronii atomului au fost comparați cu planetele sistemului solar, așa cum se poate vedea în următoarea reprezentare:
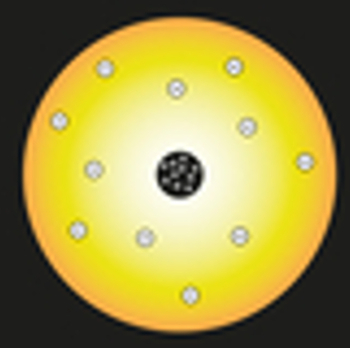
Reprezentarea modelului atomic Rutherford
În interiorul nucleului ar fi poziționate particule încărcate pozitiv, numite protoni (descoperite de Eugen Goldstein). Acest nucleu ar fi mic și dens și ar avea cea mai mare masă a atomului.
Experimentul realizat de Rutherford
Toate propunerile lui Rutherford pentru crearea modelului său atomic au fost rezultatul unui experiment în care a focalizat fascicule de radiații alfa (originate din de poloniu radioactiv prezent într-o cutie de plumb) pe o placă subțire de aur, cu o placă metalică acoperită cu sulfură de zinc în spate și pe laterale. laturi. Sulfura de zinc este o sare care, atunci când primește radiații, strălucește.
Rutherford a remarcat apoi că trei puncte (a, b, c) au strălucit în special în timpul acestui experiment:
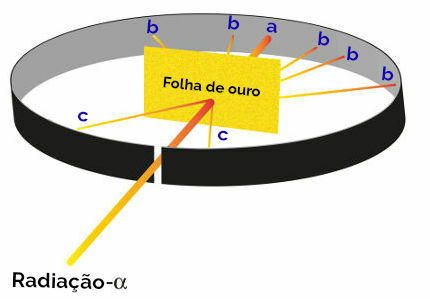
Reprezentarea experimentului Rutherford
punctul a (incidență mai mare a strălucirii): a indicat că radiația alfa a traversat placa de aur fără nicio problemă, deoarece ar fi în direcția orificiului de deschidere a blocului de plumb;
punctul b (incidență mică de strălucire): a indicat că radiația alfa a traversat placa de aur, dar că ar fi deviat în timpul traversării;
punctul c (o cantitate extrem de mică de strălucire): situată în fața lamei de aur, a indicat că radiația alfa nu a trecut.
Rutherford a atribuit aceste rezultate observate atomilor care formează placa de aur, interpretând după cum urmează:
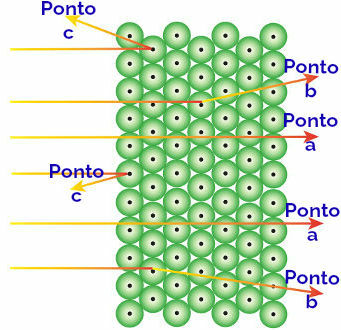
Reprezentarea comportarii radiatiilor alfa si a atomilor
Radiația alfa ajungând la arata spre: radiația alfa este pozitivă și trece printr-o regiune a atomului de spații goale uriașe. Există, de asemenea, electroni prezenți în unii orbitali.
Radiația alfa ajungând la punctul b: radiatia alfa trece prin atomii placii de aur, dar ajunge la un anumit moment cand trece aproape de nucleul mic al atomului, care este încărcat pozitiv, generând repulsie în radiatii.
Radiația alfa ajungând la punctul c: radiația alfa trece prin atomii plăcii de aur, dar lovește un nucleu mic, care este încărcat pozitiv, generând repulsie în radiație.
Problematica modelului Rutherford
Mulți fizicieni au subliniat unele probleme în modelul propus de Rutherford:
Prima problemă: cum ar fi posibil un nucleu încărcat pozitiv dacă particulele încărcate pozitiv se resping reciproc?
A doua problemă: de ce electronii din electrosfere nu sunt atrași de protonii din nucleu?
A 3-a problemă: de ce electronii, care sunt corpuri mici în mișcare continuă, nu pierd energie și nu cad în nucleu?
* Credite imagine: Svic / Shutterstock
De mine. Diogo Lopes Dias
Sursă: Brazilia școală - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-modelo-rutherford.htm


