Hibridizarea carbonului de tip sp2 apare atunci când are o legătură dublă și două legături simple sau o legătură pi (π) și trei legături sigma (σ). De fapt, hibridizarea sp2 se produce între atomii care stabilesc dubla legătură.
Un exemplu de astfel de moleculă este formaldehida (CH2O). Rețineți structura sa mai jos:
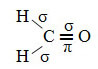
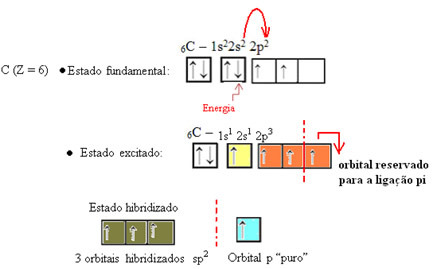
După cum se vede în text "hibridizare de tip sp3”, Hibridizarea carbonului are loc atunci când un electron din subnivelul 2 primește energie și este„ transportat ”la 2p subnivel și, astfel, originează 4 orbitali hibridizați din „amestecul” orbitalilor atomici pur.
În cazul formaldehidei, știm că va exista o legătură pi, deci unul dintre acești orbitali hibridizați este rezervat acestei legături, în timp ce celelalte trei poartă legături sigma:
Atomii de hidrogen care fac legătura unică cu carbonul, îl fac cu orbitalul lor:
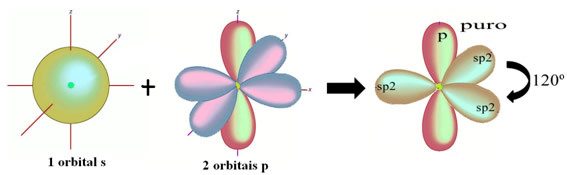
Orbitalul p „pur” rămas leagă dublu atomul de oxigen și molecula de formaldehidă are următoarea structură:
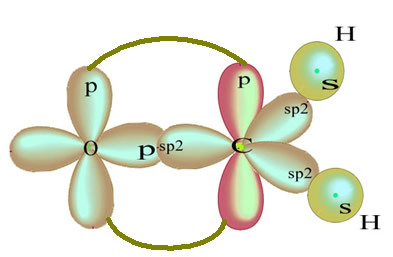
În ceea ce privește tipul de legături existente în această structură de formaldehidă, avem:

Conexiuni: 1 = 2 = σs-sp2
3 = σp-sp2
4 =πp-p
De Jennifer Fogaça
Absolvent în chimie
Sursă: Școala din Brazilia - https://brasilescola.uol.com.br/quimica/hibridizacao-tipo-sp2.htm
