Ce înseamnă să spunem că un gaz a suferit o transformare gazoasă?
Pentru a răspunde la întrebarea inițială, este important să ne amintim că starea gazului sau a stării gazoase este determinată de variabilele de stare: presiune, volum și temperatură. În curând, a transformarea gazului nu este altceva decât orice situație în care o anumită cantitate de gaz suferă variații într-una din cele trei variabile ale stării sale. Ori de câte ori o variabilă suferă modificări, o altă variabilă va avea, prin urmare, valoarea schimbată.
În secolul al XVII-lea, mai mulți oameni de știință au efectuat experimente pentru a descoperi particularitățile transformărilor de gaze. Dintre aceștia, putem menționa: Torriceli, Robert Boyle, Mariotte, Guericke, printre alții. În studiile sale, procedura a constat în schimbarea uneia dintre variabilele de stare și observarea comportamentului celorlalte. Procedând astfel, au observat că pentru a determina în mod semnificativ relația dintre o variabilă iar altul, era necesar ca al treilea să nu se schimbe, adică să rămână constant. Astfel, investigațiile au fost efectuate în trei moduri diferite, fiecare cu particularitățile sale, acestea fiind:
transformarea izotermă, transformarea izobarică și transformarea izovolumetrică.Înainte de a detalia cele trei transformări menționate mai sus, să ne amintim ce Legea generală a gazelor perfecte: Conform acestei legi, o masă de gaz definită inițial de variabile de stare (p1, V1 Si t1), când suferă o transformare gazoasă, are variabilele de stare (p2, V2 Si t2) care caracterizează starea finală a gazului. Aceste variabile urmează următoarea relație:

Din ecuația de mai sus putem vedea că presiunea, volumul și temperatura variază în timpul transformării gazului.
Transformarea izotermă sauLegea lui Boyle-Mariotte: este transformarea în care temperatura T gazului rămâne constant, variind presiunea acestuia P și volumul său V. Următoarea listă este valabilă:

Transformarea izobarică sauLegea Gay-Lussac: este transformarea în care presiunea P de gaz rămâne constant, variind volumul acestuia V și temperatura T. Următoarea listă este valabilă:
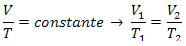
Transformarea izovolumetrică sau legea lui Charles: cunoscută și sub numele de transformare izometrică, este transformarea în care volumul V gazului rămâne constant, variind presiunea acestuia P și temperatura T. Următoarea listă este valabilă:

De Nathan Augusto
Absolvent în fizică
Sursă: Școala din Brazilia - https://brasilescola.uol.com.br/fisica/as-transformacoes-gasosas.htm


