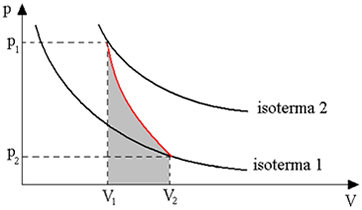
Presiunea de vapori a unui lichid este presiunea maximă exercitată de vaporii săi la atingerea echilibrului dinamic dintre fazele lichide și gazoase.
Să presupunem că aveți o substanță non-volatilă dizolvată într-un solvent volatil, de exemplu apă și sare. Se va comporta acest lichid ca și cum ar fi în stare pură? În acest caz, apa pură ar avea o tensiune maximă de vaporizare mai mare, știți de ce? Un lichid, fiind pur, se evaporă mai ușor.
Să presupunem că cantitatea de sare dizolvată din soluția de mai sus este de 10%, știm că sarea nu este volatilă și, prin urmare, tensiunea exercitată este exclusiv apă, ci în mod necesar vapori de apă. Sarea de 10% prezentă în soluție împiedică vaporizarea lichidului să fie rapidă, se determină apoi că această presiune maximă a vaporilor este cu 10% mai mică decât cea a apei pure.
Proprietatea care studiază această scădere a presiunii maxime a vaporilor cauzată de adăugarea unui dizolvat se numește Tonoscopie.
De Líria Alves
Absolvent în chimie
Echipa școlii din Brazilia
Vezi mai mult!
Presiune atmosferică - Presiunea exercitată de aer
Soluție - aspecte calitative
Soluții - Fizico-chimic
Chimie - Școala din Brazilia
Sursă: Școala din Brazilia - https://brasilescola.uol.com.br/quimica/pressao-vapor-solucoes.htm