ty estry to utlenione związki organiczne, które powstają w wyniku reakcji chemicznej między a kwas karboksylowy to jest alkohol. Przedstaw grupę funkcyjną (złożoną z dwóch atomów tlenu i dwóch radykałowie R) reprezentowane poniżej:
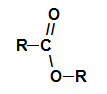
Ogólna grupa funkcyjna estru
Strukturalnie, co charakteryzuje ester jest to obecność pewnej grupy alkilowej przyłączonej bezpośrednio do atomu tlenu. W tym przypadku rodnik (R) przyłączony do węgla – który z kolei jest podwójnie przyłączony do tlenu – może być rodnikiem alkilowym lub atomem wodoru.
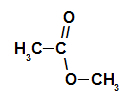
Łańcuch węglowy estru
reakcja estryfikacji
chodzi o reakcja chemiczna, w wyniku której powstaje ester i cząsteczka wody z interakcji kwasu karboksylowego z dowolnym alkoholem, jak w poniższym równaniu:
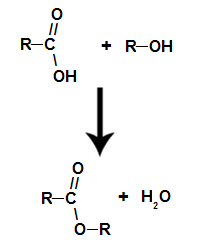
Równanie chemiczne przedstawiające tworzenie estru
Podczas estryfikacji grupa hydroksylowa (OH) alkoholu oddziałuje z wodór (H) ulega jonizacji z hydroksylu kwasu i tworzy cząsteczka wody.
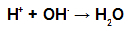
Cząsteczki wody tworzące grupy w estryfikacji
już ester powstaje przez połączenie rodnika (R) alkoholu z tlenem, który pozostaje z hydroksylu kwasu po utworzeniu wody.
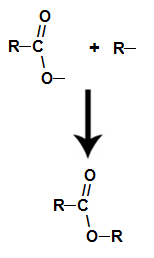
Powstawanie cząsteczki estru
Charakterystyka estrów
Główne właściwości fizyczne przedstawione przez estry:
Mają aromaty owocowe i kwiatowe;
niskie estry masa cząsteczkowa są płynne w temperaturze pokojowej, a te o dużej masie molowej są stałe;
W porównaniu z alkoholami i kwasami karboksylowymi estry mają niższe temperatury topnienia i wrzenia;
W porównaniu z wodą estry o niższej masie molowej są mniej gęste;
Estry o niższej masie cząsteczkowej są polarne, a estry o wyższej masie cząsteczkowej są niepolarne;
W estrach polarnych przeważają siły stały dipol; w niepolarnym dominują siły forces indukowany dipol;
Estry o mniejszej masie molowej są słabo rozpuszczalne w wodzie, a te o większej masie są nierozpuszczalne w wodzie.
Reguła nazewnictwa Ester
Przed użyciem zasady nazewnictwa ester, należy pamiętać, że związek ten powstaje przez połączenie dwóch części, z których jedna pochodzi od kwasu karboksylowego (na czerwono) i alkoholu (na niebiesko), co przedstawia rysunek a podążać:
Teraz nie przestawaj... Po reklamie jest więcej ;)
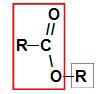
Identyfikacja części, z których powstaje ester
Według Międzynarodowej Unii Chemii Czystej i Stosowanej (IUPAC), oficjalna zasada nazywania estru to:
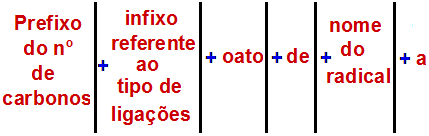
Reguła nazewnictwa Ester
Uwaga: Przedrostek i wrostek zawsze odpowiadają części kwasu karboksylowego, a rodnik odpowiada części alkoholowej.
Poniżej kilka przykładów zastosowania zasady nazewnictwa estrów:
Pierwszy przykład: esencja malinowa
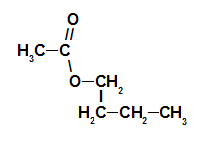
Formuła strukturalna estru esencji malinowej
Aby nazwać ten ester, używamy:
Nr PrefiksO węgli: eti, ponieważ kwas tworzący ma dwa węgle;
Infiks na typ linków: na, ponieważ kwas tworzący ma tylko pojedyncze wiązania między węglami;
scena;
w;
Rodnik: butyl, mając kolejno cztery węgle;
.
Tak więc nazwa estru odpowiadającego esencji malinowej to etanolan butylu.
Drugi przykład: esencja szyszki sosnowej
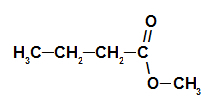
Wzór strukturalny estru szyszki sosnowej
Aby utworzyć nazwę tego estru, używamy:
Nr PrefiksO węgli: ale, ponieważ tworzący kwas ma cztery węgle;
Infiks na typ linków: na, ponieważ kwas tworzący ma tylko pojedyncze wiązania między węglami;
scena;
w;
Rodnik: metyl, ponieważ tworzący alkohol ma tylko jeden węgiel;
.
Tak więc nazwa estru odpowiadającego esencji szyszki sosnowej to butanian metylu.
Trzeci przykład: esencja truskawkowa
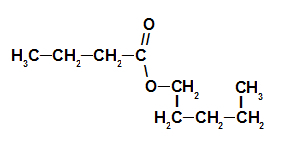
Esencja Truskawkowa Ester Wzór Strukturalny
Aby nazwać ten ester, używamy:
Nr PrefiksO węgli: ale, ponieważ kwas tworzący ma cztery węgle;
Infiks na typ linków: na, ponieważ kwas tworzący ma tylko pojedyncze wiązania między węglami;
scena;
w;
Rodnik: pentyl, ponieważ tworzący alkohol ma kolejno pięć atomów węgla;
.
Tak więc nazwa estru odpowiadającego esencji truskawkowej to butanian pentylu.
Zastosowania estrów
Estry są dobrze znane ze swojego zastosowania jako przyprawa w żywności przetworzonej, czyli substancjach, które naśladują charakterystyczny smak i aromat żywności naturalnej, np. owoców. Ponadto, estry są nadal wykorzystywane w produkcji leków, kosmetyków, perfum i wosków.
Przeze mnie Diogo Lopes Dias
Czy chciałbyś odnieść się do tego tekstu w pracy szkolnej lub naukowej? Popatrz:
DNI, Diogo Lopes. „Co to jest ester?”; Brazylia Szkoła. Dostępne w: https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-ester.htm. Dostęp 28 czerwca 2021 r.
Chemia

Estry, aromat żywności, aromat, reakcja estryfikacji, antranilan metylu, octan pentylu, etanolan butylu, butanian etylu, propanotriol, gliceryna, stearyna.
