W amidy to związki organiczne charakteryzujące się characterized obecność azot (N) bezpośrednio przyłączony do karbonylu (C=O). Są to substancje dostępne w sposób naturalny, jedna z nich znajduje się w odchodach ssaków (mocznik), ale można je również otrzymać na drodze sztucznej syntezy.
Amidy mogą być wytwarzane na przykład przez: odwadnianie soli amonowej, proces stosowany w produkcji polimerów. Są również używane jako nawozy, ze względu na dostępność azotu i jak lek o działaniu przeciwdrobnoustrojowym.
Czytaj więcej:Akrylamid – amid, który może powstać w wyniku podgrzewania niektórych produktów spożywczych
Struktura amidowa
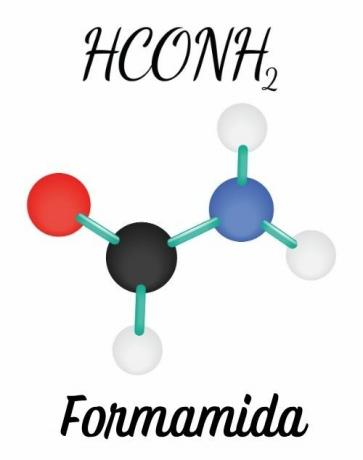
Amidy są tworzone przez azot związany bezpośrednio z grupą karbonylową lub acylową (R-C=O). Podwójne wiązanie między węgiel to jest tlen a możliwość przeniesienia tej pary do azotu dają cząsteczce geometria planarna, w przeciwieństwie do amin, które mają geometrię piramidalną.
Klasyfikacja amidów
Klasyfikacja według liczby podstawników organicznych
Tak dobrze jak aminyamidy są klasyfikowane zgodnie z liczba zastępujących rodników organicznych, które ma azotjednak dla amidów musimy wziąć pod uwagę, że jednym z ligandów grupy będzie grupa acylowa, czyli będziemy mieli tylko amidy typu:
- Niepodstawiony amid: ma azot związany z dwoma wodory i grupę karbonylową.
Przykład:

- Amina monopodstawiona: zawiera azot związany z wodorem, grupą karbonylową i rodnikiem organicznym. W tym przypadku, gdy jeden z wodorów został zastąpiony łańcuchem węglowym, rozważ R jako grupę organiczną.
Przykład:

- Amina dipodstawiona: ma azot związany z dwoma rodnikami organicznymi i karbonylem. W tym przypadku dwa wodory zostały zastąpione łańcuchami węglowymi.
Przykład:

Zobacz też: Jak klasyfikować halogenki organiczne?
Klasyfikacja według liczby karbonylków związanych z azotem
Amidy można również klasyfikować według liczby karbonyli przyłączonych bezpośrednio do azotu cząsteczki.
- Amidy pierwszorzędowe: tylko jedna grupa acylowa połączona z azotem (R-CO)NH2 .
- amidy drugorzędowe: dwa karbonylki lub grupy acylowe połączone z azotem (R-CO)2NH.
- trzeciorzędowe amidy: trzy grupy acylowe połączone z azotem (R-CO)3Nie.

Nomenklatura amidów
TEN nomenklatura amidów udzieli:
przedrostek wskazujący liczbę węgli w łańcuchu + położenie i wrostek wskazujący nienasycenia (jeśli występują) + zakończenie amidowe |
Zobacz tabelę poniżej:
Prefiks (liczba węgli) |
Infix (nasycenie łańcucha) |
Sufiks (grupa funkcyjna) |
|||
1 węgiel |
Spotkał- |
Tylko pojedyncze połączenia |
-na- |
amidy |
-amid |
2 węgle |
Et- |
||||
3 węgle |
Rekwizyt- |
1 podwójne wiązanie |
-pl- |
||
4 węgle |
Ale- |
||||
5 węgli |
zamknięty- |
2 podwójne wiązania |
-dien- |
||
6 węgli |
Klątwa- |
||||
7 węgli |
Hept- |
1 potrójne wiązanie |
-w- |
||
8 węgli |
Październik- |
||||
9 węgli |
Nie- |
2 potrójne ogniwa |
-diin- |
||
10 węgli |
Dec- |
Liczenie węgla musi zaczynać się od strony najbliższej azotowi grupy funkcyjnej.
Przykłady:
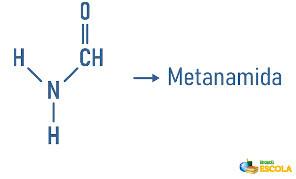



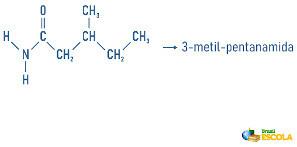
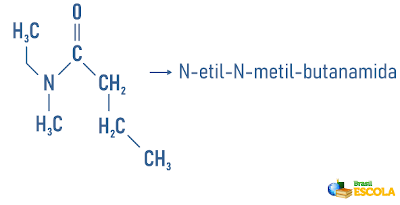
Aminy mogą również otrzymać w swojej nomenklaturze specyfikację dotyczącą klasyfikacji cząsteczki:
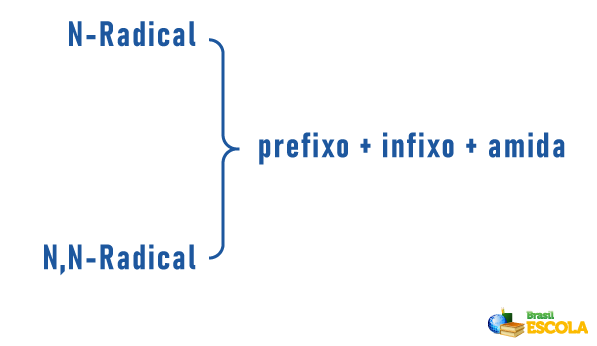
Pamiętając, że nomenklaturę dla rodników tworzą: Prefix wskazujący liczbę węgli + zakończenie „il” lub „ila”. Radykały są umieszczone w nomenklaturze w porządku alfabetycznym.
Przykłady:


Również dostęp: Nomenklatura węglowodorów cyklicznych i rozgałęzionych
Właściwości amidów
- Wysoka temperatura topnienia i wrzenia, która będzie miała wartość skalowaną zgodnie z rozmiarem i przestrzennym układem łańcucha węglowego.
- Wysoce polarny ze względu na obecność karbonylu i azotu.
- Wiązanie wodorowe amidów niepodstawionych i monopodstawionych.
- Mniejsze i prostsze cząsteczki są rozpuszczalne w wodzie. Rozmiar cząsteczki wpływa również na rozpuszczalność amidów: im większy łańcuch węglowy, tym mniej będą one rozpuszczalne w wodzie.
- Amidy są podstawowe ze względu na skłonność do przyjmowania jonów H+.
Zastosowanie amidów
- Używany jako pośrednicy w produkcji polietylenów, takich jak nylon.
- Stosowany w formulacji leków takich jak sulfanilamid i penicylina, aktywnych składników leków bakteriobójczych do kontroli infekcji.
- Mocznik, który można otrzymać syntetycznie lub jako produkt wydalany przez ssaki, jest substancją z grupy amidowej, diamidem. Stosowany jest jako suplement diety w rolnictwie oraz jako nawóz.

Otrzymywanie amidów
Amidy łatwo znaleźć w postaci naturalnej, ale ich postać syntetyczna jest nadal szeroko stosowana w procesach przemysłowych. Poniżej przedstawiono niektóre reakcje produkcji amidów w oparciu o inne związki azotowe.
Reakcja odwadniania soli amonowej

Reakcja amin z chlorkiem kwasowym
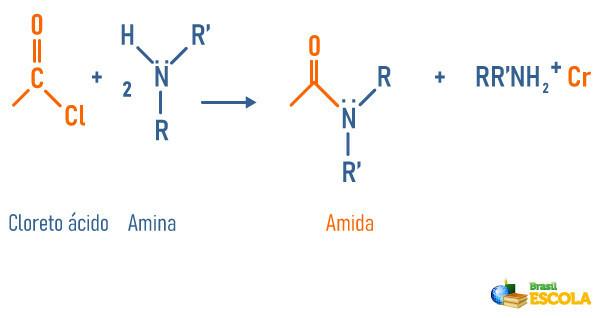
-
Reakcja bezwodników z aminami
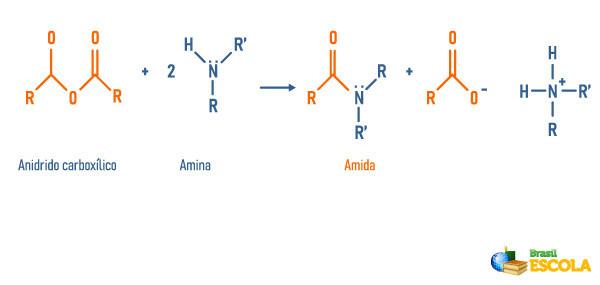
Reakcja estrów z aminami

Przegrupowanie strukturalne aldoksymu
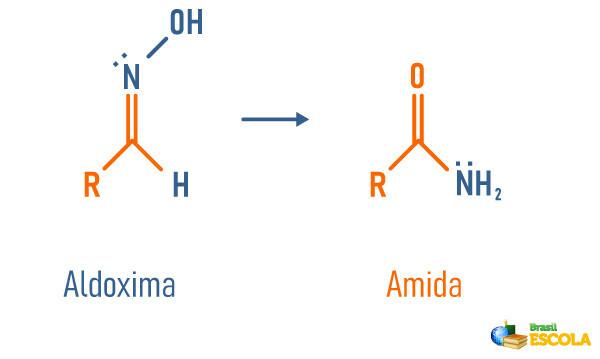
-
Nawodnienie nitrylowe
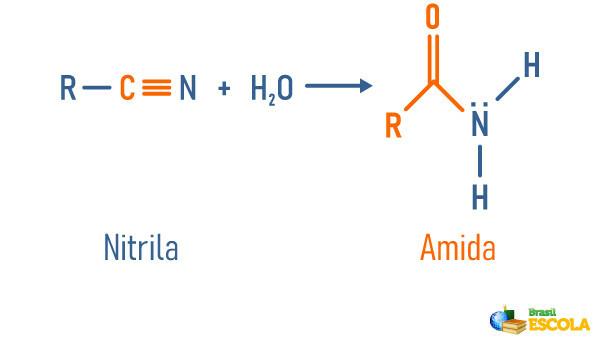
Przeczytaj też: Hydroliza amidowa - reakcja stosowana do otrzymywania ważnych substancji
rozwiązane ćwiczenia
Pytanie 1 - (UFRS) Aspartam, przedstawiony poniżej, jest sztucznym słodzikiem stosowanym w wielu napojach bezalkoholowych i niskokalorycznej żywności.

Grupa obramowana na rysunku jest charakterystyczna dla funkcji organicznej
A) ester.
B) amid.
C) aminokwas.
D) amina.
E) węglowodan.
Rozkład
Alternatywa B. Wybraną na figurze grupą funkcyjną jest amid, ze względu na obecność grupy karbonylowej (C=O) połączonej bezpośrednio z azotem (N).
Pytanie 2 - (UNESP) W sierpniu 2005 r. zgłoszono konfiskatę partii lidokainy, która spowodowałaby śmierć kilku osób w Brazylii z powodu problemów produkcyjnych. Lek ten jest miejscowym środkiem znieczulającym szeroko stosowanym w badaniach endoskopowych, zmniejszając dyskomfort pacjenta. Jego strukturę molekularną pokazano poniżej:
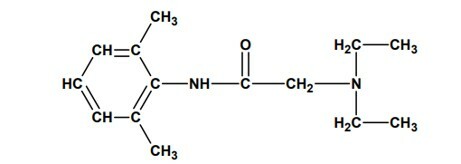
i przedstawia funkcje:
A) amina drugorzędowa i amina trzeciorzędowa.
B) amid i trzeciorzędowa amina.
C) amid i ester.
D) ester i trzeciorzędowa amina.
E) ester i drugorzędowa amina.
Rozkład
Alternatywa B.
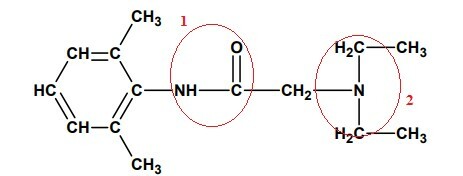
Po wybraniu i ponumerowaniu charakterystycznych części każdej funkcji organicznej przeanalizujmy każdą z nich:
1- Jest to AMIDA ze względu na obecność grupy acylowej (R-C=O) bezpośrednio związanej z azotem, monopodstawionej.
2- Ponieważ nie mamy obecności grupy acylowej (R-C=O), a jedynie azot związany bezpośrednio z innymi węglami w tej grupie mamy trzeciorzędową aminę, ponieważ wszystkie trzy wodory, wcześniej związane z azotem, zostały zastąpione grupami Organiczny.
Laysa Bernardes Marques de Araújo
Nauczyciel chemii

