Aminy to związki organiczne powstające w wyniku zastąpienia jednego lub więcej wodorów z amoniaku (NH3) przez grupy organiczne. Symbolizując te rodniki przez R, mamy, że ich grupę funkcyjną można zidentyfikować na trzy poniższe sposoby:
R ─ NH2 lub R NH ─ R’ lub R─N─R’
│
R"
Związki należące do tej funkcji organicznej są bardzo ważne w naszym codziennym życiu i we własnym organizmie, pełnią bardzo ważne funkcje biologiczne, ponieważ występują w aminokwasach tworzących podstawowe białka dla żyjące istoty.
Są również szeroko stosowane przemysłowo, np. w wulkanizacji gumy, w produkcji mydeł, leków oraz w niezliczonych syntezach organicznych. Wiele, niestety, jest używanych jako narkotyki.
W związku z tym wiele amin jest często znanych pod nazwami zwyczajowymi. Zobacz kilka przykładów:
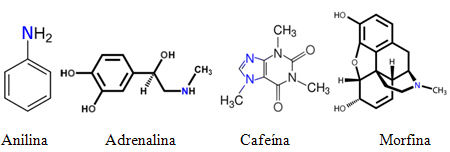
Nie jest jednak możliwe, aby wszystkie znane aminy były nazywane tylko nazwami zwyczajowymi podobnymi do wymienionych. Potrzebne są zasady nazewnictwa, aby każdy na świecie mógł przeprowadzać eksperymenty z tą samą substancją, aby jego struktura była łatwa do zidentyfikowania poprzez nazwę i nawzajem.
W związku z tym IUPAC ustalił, że nomenklatura amin musi być zgodna z następującą zasadą:
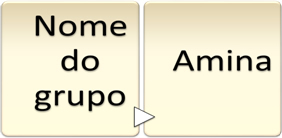
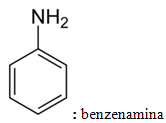
Ta zasada dotyczy tylko aminy pierwszorzędowe, czyli w którym tylko jeden atom wodoru amoniaku został zastąpiony przez rodnik o następującej grupie funkcyjnej: R ─ NH2.
Przykłady:
H3C NH2: metanamina
H3C CH2 NH2: etanoamina
H3C CH2 CH2 CH2 NH2: butano-1-amina
Gdy w łańcuchu występują rozgałęzienia lub nienasycenia, konieczne jest numerowanie łańcucha od najbliższego końca grupy NH2 i pokaż w jakim węglu występuje:
NH2
│
H3C ─ CH ─ CH2 CH2 CH2 CH3: heksano-2-amina
NH2
│
H3C CH2 CH2 ─ C ═ CH ─ CH3: heks-2-en-3-amina
CH3 NH2
│ │
H3C CH ─ CH ─ CH2 CH3: 2-metylo-pentano-3-amina
CH3 NH2
│ │
H3C ─ CH ─ CH2 CH─CH3: 4-metylo-pentano-2-amina
W przypadku aminy drugorzędowe i trzeciorzędowe (które mają odpowiednio dwa i trzy podstawione wodory grupy amonowej), zasada jest inna:

Nazwy tych amin są poprzedzone literą N, aby wskazać, że podstawnik jest przyłączony do atomu azotu, a podstawniki w łańcuchu węglowym są zwykle oznaczone cyframi.
Przykłady:
H3C CH2 CH2 ─ NH ─ CH2: N-metylopropanamina
CH3 CH3
│ │
H3C ─ CH ─ CH2 ─ NIE ─ CH2 CH3: N-etylo-2,N-dimetylopropanamina
H3C─N─CH2 CH3: N-dimetylo-etanoamina
│
CH3
H3C─N─CH2 CH3: N-metylo-etano-1-amina
│
H
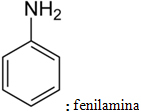
Istnieją dwa rodzaje zwykła nomenklatura dla amin. Pierwszy jest zgodny z następującym schematem:

Przykłady:
H3C NH2: metyloamina
H3C CH2 NH2: etyloamina
H3C CH2 CH2 CH2 NH2: butyloamina
H3C─N─CH2 CH3: etylodimetyloamina
│
CH3
H3C─N─CH2 CH3: etylometyloamina
│
H
H3C─N─CH3: trimetyloamina
│
CH3
Trimetyloamina jest głównym składnikiem nieprzyjemnego zapachu zgniłych ryb.
Inny zwykła nomenklatura rozważ grupę NH2 jako gałąź łańcucha węglowego i jest wskazywana przez przedrostek “amino”. Najdłuższy łańcuch jest głównym, a reszta to gałąź. Zobacz przykłady:
CH3 CH3
│ │
H3DO1 C2 C3H ─C4H2 C5H3: 2-amino-2,3-dimetylo-pentan
│
NH2
CH2 CH2 CH2 CH2 : 1,4-diamino-butan
│ │
NH2 NH2
CH2 CH2 CH2 CH2 CH2 : 1,5-diaminopentan
│ │
NH2 NH2
Te dwa ostatnie związki są znane w życiu codziennym odpowiednio jako putrescyna i kadaweryna, aminy, które powstają podczas rozkładu ludzkich zwłok.
Jennifer Fogaça
Absolwent chemii
Źródło: Brazylia Szkoła - https://brasilescola.uol.com.br/quimica/nomenclatura-das-aminas.htm

