ty metale są to pierwiastki chemiczne, których główną cechą fizyczną jest zdolność do utraty elektronów, a w konsekwencji do tworzenia kationów metali. Z tego powodu mogą tworzyć dwa rodzaje wiązań chemicznych: wiązanie jonowe i wiązanie metaliczne.
TEN wiązanie jonowe występuje, gdy metal wchodzi w interakcję z elementem o charakterze metalicznym, który może być ametal lub wodór. W tym typie wiązania mamy do czynienia z utratą elektronów przez metale i pozyskiwaniem elektronów przez niemetale lub wodór.
już wiązanie metaliczne ustala się między atomami pojedynczego pierwiastka metalicznego. Ten rodzaj wiązania występuje tylko między atomami jednego metalu i wyłącznie dlatego, że metal nie może ustanowić wiązania chemicznego z innym innym pierwiastkiem metalicznym.
Ogólna charakterystyka metali
Ciała stałe w temperaturze pokojowej, z wyjątkiem rtęci;
Są genialne;
Mają wysoką temperaturę topnienia i wrzenia;
Zazwyczaj są koloru srebrnego, z wyjątkiem złota, które jest złote i miedzi, które jest czerwonawe;
Czyste metale tworzą skupiska atomów (jednego pierwiastka chemicznego) zwane sieciami krystalicznymi.
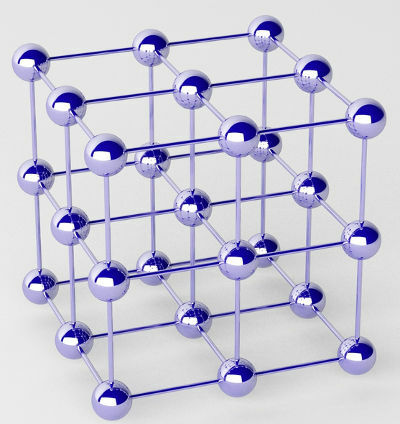
Reprezentacja sieci krystalicznej metalu
Zasady wiązania metalicznego
W wiązanie metaliczne, sieci krystaliczne, które tworzą metale, są w rzeczywistości klastrem jonowym (składającym się tylko z kationy i elektrony). Elektrony obecne w warstwie walencyjnej atomów metalu ulegają delokalizacji, to znaczy opuszczają warstwę walencyjną, powodując, że atom staje się kationem (z niedoborem elektronów).
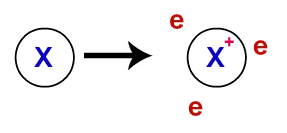
Reprezentacja zdelokalizowanych elektronów z powłoki walencyjnej
Po delokalizacji elektrony z atomów metalu zaczynają otaczać kationy, tworząc prawdziwe „morze elektronów”. Każdy z elektronów obecnych w tym morzu ma zdolność swobodnego poruszania się po sieci krystalicznej metalu.

Reprezentacja modelu morza elektronowego
UWAGA: Elektrony „z morza” nie są w stanie opuścić sieci krystalicznej i przejść przez nią.
Właściwości metali uzasadnione wiązaniem metalicznym
a) Plastyczność
Dzięki metalowi można wytwarzać arkusze o różnych grubościach i arkuszach. To właśnie dzięki tej właściwości metali możemy budować różne przedmioty, takie jak noże, miecze itp.

Ostrze miecza wykonane jest z metalu
b) Przewodność
Ogólnie rzecz biorąc, metale są dobrymi przewodnikami prądu elektrycznego i ciepła. Kiedy jakikolwiek metal styka się ze źródłem ciepła lub źródłem prądu elektrycznego, jest w stanie je przewodzić.

Aluminiowa patelnia w płomieniu pieca nagrzewa się całkowicie z powodu przewodnictwa.
c) Ciągliwość
Poprzez metal możemy produkować druty. Zastosowanie metalu w postaci drutów ułatwia jego użycie, zwłaszcza w odniesieniu do przewodności elektrycznej.

Do produkcji przewodów można użyć metalu, takiego jak miedź.
Przeze mnie Diogo Lopes Dias
Źródło: Brazylia Szkoła - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-ligacao-metalica.htm
