TEN stała jonizacji daje woda(Kw), O potencjał wodorowy(pH) to jest potencjał hydroksylowy (pOH) oni są środki ważne dla obliczeń obejmujących równowaga chemiczna w roztworach kwaśnych i zasadowych oraz przy oznaczaniu stężenia jonów H+ i och- kwestionowanych rozwiązań.
Co to jest Kw?
Jonowy iloczyn wody lub Kw (to ( wznaczy woda — woda, w języku angielskim) jest stałą używaną do reprezentowania równowaga generowana przez samojonizację wody. Nawet przy bardzo małej szybkości woda jonizuje wytwarzając jony H+ i och-, zgodnie z następującym równaniem chemicznym:
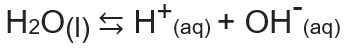
Analizując równanie, zdajemy sobie sprawę, że gdy jonizacja z cząsteczki czystej wody generowany jest jon H.+ i jon OH-, to jest stężenie tych jonów zawsze będzie takie samo. Nawet w przypadku wzrostu temperatury, który powoduje wzrost szybkości jonizacji, stężenia pozostają takie same.
Przeczytaj też:Energia jonizacji
Na podstawie pomiarów doświadczalnych obliczono stężenie jonów H+ i och- (wynikająca z samojonizacji wody) w temperaturze 25°C i wartości
1. 10-7 mol/L. To jest, łącznie 1 miliarda cząsteczek wody, tylko dwa przechodzą jonizację. To pokazuje, że czysta woda ma niski stopień jonizacji i wyjaśnia bardzo niski Przewodność elektryczna czystej wody.Biorąc pod uwagę to, co zostało pokazane powyżej, możemy napisać wyrażenie stałej bilansu wodnego:

Przy użyciu wartości stężenia jonów H+ i och- w 25°C możemy obliczyć wartość Kw:
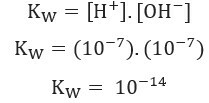
Jak wspomniano wcześniej, ta wartość Kw zmienia się wraz ze wzrostem temperatury, jak pokazano w poniższej tabeli:
T (°C) |
Kw |
10 |
0,29. 10-14 |
20 |
0,68. 10-14 |
25 |
1,00. 10-14 |
30 |
1,47. 10-14 |
40 |
2,92. 10-14 |
60 |
9,40. 10-14 |
Aby dowiedzieć się więcej na ten temat, przeczytaj nasz tekst: Produkt w postaci wody jonowej.
Co to jest pH i pOH?

akronim pH znaczy potencjał wodorowy i został stworzony przez duńskiego biochemika Soren Sorensen, w 1909 roku, aby ułatwić pracę z stężenia jonów wodorowych [H+], które są zwykle wyrażane w liczbach dziesiętnych. Aby dowiedzieć się więcej na ten temat, przeczytaj nasz tekst: Co to jest pH?
Ten rodzaj notacji wskazuje zawartość jonów H+ obecny w rozwiązaniu i jest zdefiniowany przez wyrażenie matematyczne:
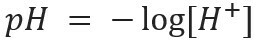
Podobnie możemy zdefiniować pOH lub potencjał hydroksyjonowy, który mówi nam Zawartość jonów OH- obecny w rozwiązaniu. Jego matematyczne wyrażenie to:
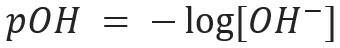
W roztworze wodnym zawsze będą jony H+ i och- (ze względu na jonizację wody), który zostanie wykorzystany do scharakteryzowania roztworu w kwaśny lub podstawowy. Im więcej jonów H+ jest w roztworze, tym bardziej będzie kwaśny. W konsekwencji obecność jonów OH- w rozwiązaniu sprawi, że będzie bardziej podstawowy. Jeśli istnieje równowaga w ilości tych jonów, roztwór zostanie sklasyfikowany jako neutralny.
Skala pH
Wyświetlana jest skala pH z wartościami z zakresu od 0 do 14 (wartości mierzone przy 25°C). Zobacz skalę pH na poniższym obrazku:

Im niższe pHrozwiązania,większa jest jego kwasowość, a im bliżej końca skali, czyli bliżej 14, tym większy jest jej podstawowy charakter. Na przykład sok z cytryny ma pH 2, a wybielacze mają pH 12.
Jak obliczyć pH i pOH
znając stężenie jonów, możemy obliczyć wartości pH i pOH roztworów i znając potencjalne wartości obliczamy stężenie jonów w roztworach. W tym celu używane są następujące wyrażenia:
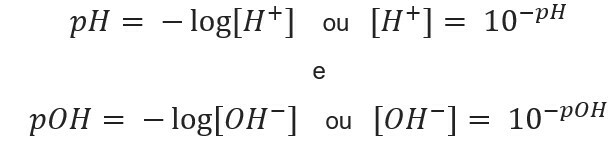
Przejdźmy do przykładów:
Przykład 1
Jeśli chcemy poznać pH roztworu z [H+] = 0,001 mol/L, wystarczy skorzystać z wcześniej przedstawionego wzoru:
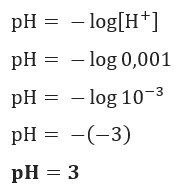
Przykład 2
Teraz, aby dowiedzieć się, jakie jest stężenie OH- roztworu o pOH = 5, wystarczy zastąpić wartość w następującym wzorze:

Jeśli zastosujemy tę samą skalę potencjałów do równowagi jonowej wody, otrzymamy:
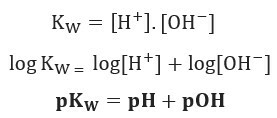
Jak stwierdzono, w 25°C Kw = 10-14. W związku z tym:

Dzięki temu możemy obliczyć pOH roztworu na podstawie jego pH. Jeśli mamy roztwór o pH 3, to jego pOH wyniesie 11.
Wiedzieć więcej: Media neutralne, kwaśne i zasadowe
rozwiązane ćwiczenia
Pytanie 1 (UEFS-BA) Stężenie jonów OH–(tutaj) w danym roztworze wodorotlenku amonu w temperaturze 25 °C wynosi 1,10–3 mol/L. Wartość pOH tego rozwiązania wynosi:
a) 0
b) 1
c) 3
d) 11
e) 13
Rozkład: Litera C. Jeśli mamy [OH–] = 10–3 mol/L, więc twój pOH będzie równy 3.
Popatrz:
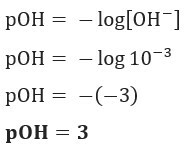
Pytanie 2 (UEA-AM) Weź pod uwagę następujące informacje, uzyskane z etykiety wody mineralnej w mieście Porto Seguro (BA):
azotan 1,45 mg/L
pH w 25°C 4,51
Ta woda mineralna jest
a) kwaśny i ma [H+] < [OH–].
b) kwaśny i ma [H+] > [OH–].
c) neutralny i ma [H+] = [OH–].
d) podstawowy i ma [H+] > [OH–].
e) podstawowy i ma [H+] < [OH–].
Rozkład: Literka B. Ponieważ pH wody mineralnej podane na etykiecie jest mniejsze niż 7, możemy powiedzieć, że jest to roztwór kwaśny, a co za tym idzie stężenie jonów H+ jest większy niż OH-.
Pytanie 3 (UEA-AM) Jednym ze sposobów szybkiego wytworzenia gazowego wodoru w laboratorium jest reakcja sproszkowanego metalicznego cynku z kwasem solnym (HCl) o stężeniu 1,0 mol/L:
Zn (s) + 2 HCl (aq) → ZnCl2 (aq) + H2 (sol)
Biorąc pod uwagę, że kwas solny jest w 100% zjonizowany, a roztwór ma temperaturę 25°C, prawidłowe jest stwierdzenie, że pH roztworu kwasu solnego wymienionego w tekście jest
- 0
- 1
- 3
- 13
- 14
Rozkład:Litera a. Wartość pH roztworu możemy obliczyć na podstawie podanego w tekście stężenia HCl, ponieważ ponieważ jest on w 100% zjonizowany, stężenie [H+] będzie taka sama, ponieważ na każdą zjonizowaną cząsteczkę HCl przypada jeden jon H+ zostanie wygenerowany. W związku z tym:
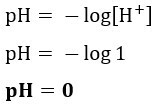
Autor: Victor Ferreira
Nauczyciel chemii
