Skoro istnieją wyjątki od reguły oktetów, skąd możemy poznać prawidłowe ułożenie atomów podczas tworzenia cząsteczki?
Można to zrobić, obliczając formalne obciążenie każdej konstrukcji. Ładunek formalny najbliższy zeru będzie tym o największym prawdopodobieństwie rzeczywistego istnienia. Zwróć uwagę, że jest „najbliżej zera”, więc nie musi to być zero.
Formalna formuła ładunku (Cfo) é:
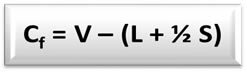
V = liczba elektronów walencyjnych wolnego atomu;
L = liczba elektronów obecnych w izolowanych (niewiążących) parach atomu w strukturze;
S = liczba elektronów wspólnych dla atomu w strukturze.
Aby zrozumieć, jak to się dzieje, wyobraź sobie, że chcemy wiedzieć, jaka jest struktura elektronowa Lewisa dla cząsteczki SO.2. Mamy dwa możliwe układy między atomami:
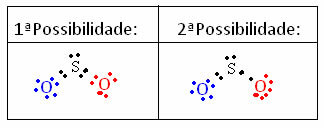
Obliczany jest ładunek formalny wszystkich atomów uczestniczących w strukturach. Popatrz:
1. możliwość:
Siarka(S): Tlen (O) Tlen (O)
DOf(S) = 6 – (2 + ½ 8) DOf(S) = 6 – (4 + ½ 4) DOf(S) = 6 – (4 + ½ 4)
DOf(S) =0 DOf(S) =0 DOf(S) =0
Druga możliwość:
Siarka(S): Tlen (O) Tlen (O)
DOf(S) = 6 – (2 + ½ 6) DOf(S) = 6 – (6 + ½ 2) DOf(S) = 6 – (4 + ½ 4)
DOf(S) = +1DOf(S) = -1 DOf(S) =0
Na podstawie uzyskanych wyników możemy zauważyć, że pierwsza struktura to ta o najwyższym prawdopodobieństwie rzeczywistego istnienia. Wiemy więc, że nie jest to reguła oktetu, ale siarka rozszerzyła swoją powłokę walencyjną, pozostając stabilną z 10 elektronami.
Ta zasada dotyczy również znalezienia prawidłowego ułożenia jonów.
Jennifer Fogaça
Absolwent chemii
Źródło: Brazylia Szkoła - https://brasilescola.uol.com.br/quimica/calculo-carga-formal.htm

