Jeden reakcja dodawania to proces chemiczny, w którym atomy substancji nieorganicznej są dodawane do cząsteczki organicznej, która musi mieć jedną z następujących cech:
Otwarta struktura zawierająca wiązanie lub pi linki;
Nasycona struktura zamknięta (tylko z linki sigma);
Zamknięta struktura nienasycona (z wiązaniem pi lub aromatycznym).
Związki organiczne, które mają te cechy, są następujące Węglowodory:
alkeny;
Alkiny;
Alkadieny;
Cyklany;
Cykle;
Aromaty.
Podczas reakcja dodawania, jedno lub więcej wiązań pi lub wiązanie sigma (w wyłącznym przypadku cyklanu) są zerwane powodując pojawienie się dwóch lub więcej wolnych wartościowości (miejsc wiązania) na zaangażowanych węglach, jak w przykładzie poniżej:
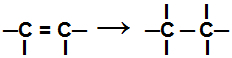
Zerwanie wiązania pi w alkenach
Po zerwaniu tego wiązania, dodanie atomów musi nastąpić w nowych miejscach wiązania utworzonych w związku organicznym. Poniżej wymieniamy rodzaje reakcje dodawania które można przeprowadzić za pomocą związków organicznych.
uwodornienie
W tym reakcja dodawania, oprócz związku organicznego, drugim reagentem jest gazowy wodór (H
2). W każdym z węgli, gdzie następuje rozszczepienie (zerwanie wiązania sigma lub pi, jak widać wcześniej), będzie wiązanie atomu wodoru odnoszące się do ilości zerwanych wiązań.Kiedy przeprowadzamy uwodornienie cyklobutanu, na przykład, wiązanie sigma zostaje zerwane między węglem 1 i 2. Następnie atom wodoru wiąże się z każdym z tych węgli:
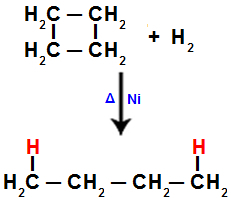
Równanie przedstawiające uwodornienie w cyklobutanie
Halogenacja
Oprócz związku organicznego drugi odczynnik w tym reakcja dodawania jest cząsteczkowym halogenem (gaz chlor-Cl2, gaz fluorowy-F2, stały jod-I2 i ciekły brom-Br2). Na każdym węglu, gdzie następuje rozszczepienie (zrywanie wiązania sigma lub pi, jak widać powyżej), będzie wiązanie atomu fluorowiec odnosząc się do liczby zerwanych połączeń.
Tak więc, gdy przeprowadzamy halogenowanie (za pomocą gazowego chloru) cyklopropenu, wiązanie pi zostaje zerwane między węglem 1 i 2. Następnie atom chloru wiąże się z każdym z tych węgli:

Równanie przedstawiające halogenowanie w cyklopropen
Reakcja addycji z halogenkiem
Halogenek jest nieorganicznym kwasem hydraulicznym utworzonym przez atom wodoru i atom wodoru. halogen, taki jak kwas solny (HCl), kwas fluorowodorowy (HF), kwas bromowodorowy (HBr), kwas jodowodorowy (HI).
W reakcja dodawania z halogenkiem, oprócz związku organicznego, drugim odczynnikiem jest halogenek, stąd jeden z węgli, gdzie scission (zerwanie wiązania sigma lub pi, jak widać powyżej), musi otrzymać atom wodoru, a drugi otrzymuje halogenek.
Według Reguła Markownikowa, najbardziej uwodorniony atom węgla (lub węgiel przyłączony do mniejszego rodnika) musi otrzymać wodór, a mniej uwodorniony węgiel (lub węgiel przyłączony do większego rodnika) musi otrzymać halogenek.
Na przykład, gdy przeprowadzamy tę reakcję na propenie z kwasem chlorowodorowym (HCl), wiązanie pi zostaje zerwane między węglem 1 i 2. Następnie wodór wiąże się z węglem 1 (bardziej uwodornionym), a chlor z węglem 2 (mniej uwodornionym):
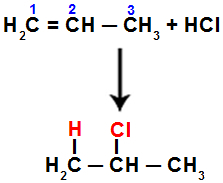
Równanie przedstawiające addycję z halogenkiem w propenie
Reakcja hydratacji
Cząsteczka wody podczas jonizacji wytwarza kation hydroniowy (H+) i anion wodorotlenkowy (OH-). Z tego powodu w tym reakcja dodawania, oprócz związku organicznego, drugim reagentem jest woda. Tak więc jeden z węgli, w którym następuje rozszczepienie (zrywanie wiązania sigma lub pi, jak widać powyżej), otrzymuje kation hydroniowy, a drugi anion wodorotlenowy.
Zgodnie z regułą Markownikowa najbardziej uwodorniony atom węgla (lub węgiel przyłączony do mniejszego rodnika) musi otrzymać hydronium, a mniej uwodorniony węgiel (lub węgiel przyłączony do większego rodnika) musi otrzymać wodorotlenek.
Kiedy na przykład uwodnimy penta-1,4 dien, wiązanie pi zostaje zerwane między węglami 1 i 2 oraz między węglami 4 i 5. Następnie węgle 1 i 5 otrzymują hydron, a węgle 2 i 4 otrzymują wodorotlenek:
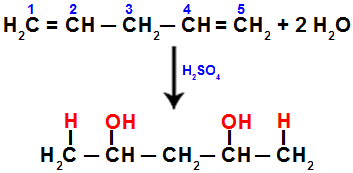
Równanie przedstawiające addycję z uwodnieniem w penta-1,4 dienie
Przeze mnie Diogo Lopes Dias
Źródło: Brazylia Szkoła - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-reacao-adicao.htm


