Reakcje przemieszczenia, nazywany również reakcje podstawienialub jeszcze z prosta wymiana, to te, które występują, gdy prosta substancja (utworzona przez pojedynczy pierwiastek) reaguje z substancją złożoną, „wymieniając” ją w nową prostą substancję.
Ogólnie możemy to zdefiniować w następujący sposób:
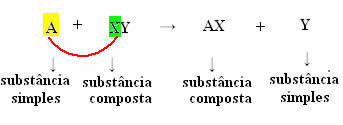
Ale żeby tak się stało, prosta substancja, w przypadku symbolizowanym przez A, musi być bardziej reaktywny niż pierwiastek, który zostanie wyparty ze związku, przekształcając się w nową prostą substancję (Y).
Spójrzmy na przykład, w którym zachodzi ta reakcja:
Obserwuj poniższy eksperyment, w którym arkusz cynku (Zn) jest umieszczany w wodnym roztworze siarczanu miedzi (CuSO4). Z biegiem czasu można zauważyć, że roztwór siarczanu miedzi zmienia kolor z niebieskiego na mniej intensywny niebieski, ponieważ odbarwił się i na blasze cynkowej pojawił się osad miedzi.

Możemy przedstawić tę reakcję za pomocą następującego równania chemicznego:

Zauważ, że cynk wyparł miedź, co oznacza, że cynk jest najbardziej reaktywny.
Ponieważ oba są metalami, możemy sprawdzić, czy nastąpi prosta reakcja wymiany, czy nie, analizując kolejka reaktywności metalu pokazane poniżej:

Zwróć uwagę, że miedź jest w rzeczywistości mniej reaktywna niż cynk, więc jeśli zdecydowaliśmy się zrobić coś przeciwnego niż w poprzednim eksperymencie i umieścić blachę miedzianą w roztworze siarczanu cynku, reakcja nie zaszłaby, ponieważ miedź nie byłaby w stanie wyprzeć cynk.
Reakcje przemieszczenia są rodzajem reakcji redoks, ponieważ następuje przeniesienie elektronów z prostej substancji do kompozytu. W opisanym powyżej procesie cynk był początkowo w swojej neutralnej postaci, która jest metaliczna i stał się częścią związku, w którym ma ładunek 2+, czyli każdy atom cynku stracił dwa elektrony. W przypadku miedzi dzieje się odwrotnie, otrzymuje ona dwa elektrony, które przechodzą do metalicznego, stałego stanu.
W przypadku prostej reakcji wymiany z niemetalami jest to rozważane: reakcja zajdzie tylko wtedy, gdy najbardziej reaktywny niemetal jest prostą substancją, która może wyprzeć inny mniej reaktywny niemetal. Reaktywność ametali pokazano poniżej:

Jennifer Fogaça
Absolwent chemii
Źródło: Brazylia Szkoła - https://brasilescola.uol.com.br/quimica/reacoes-deslocamento-substituicao-ou-simples-troca.htm
