Tekst "Cząsteczka z asymetrycznymi izomerami węgla i optycznymi” pokazał, że gdy cząsteczka ma tylko jeden asymetryczny lub chiralny węgiel (ze wszystkimi ligandami) różnią się od siebie), ma dwa optycznie czynne izomery i jeden optycznie nieaktywny izomer (mieszanina racemiczny).
Rozważmy teraz przypadek, w którym istnieją dwa lub więcej różnych asymetrycznych atomów węgla, to znaczy są one uważane za różne od siebie, ponieważ co najmniej jeden z ich ligandów nie jest taki sam. Rozważmy na przykład formułę aspartamu, który jest 180 razy słodszy niż sacharoza (cukier) i dlatego jest stosowany w sztucznych słodzikach:
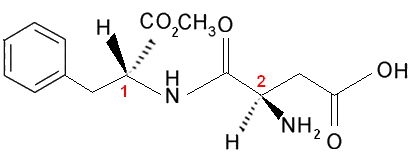
Zauważ, że ta cząsteczka ma dwa chiralne węgle, które są identyfikowane na obrazku za pomocą liczb 1 i 2. Te węgle mają swoje cztery grupy wiążące różniące się od siebie, więc są uważane za asymetryczne. Porównując ligandy węglowe 1 z tymi węglowymi 2widzimy, że jedynym powtarzającym się ligandem jest H (wodór), będący zatem różnymi asymetrycznymi atomami węgla.
Ta cząsteczka i wszystkie te, które mają dwa asymetryczne węgle, zawsze będą miały:
4 optycznie czynne izomery i 2 optycznie nieaktywne izomery (dwie mieszaniny racemiczne).Wiemy o tym, ponieważ możliwe prawdopodobieństwa to:

Wszelkie inne pary izomerów będą diastereoizomerami (które nie są swoimi lustrzanymi odbiciami), takimi jak mieszanina prawoskrętnego węgla-1 i prawoskrętnego węgla-2.
Byłoby jednak bardzo trudno, gdybyśmy musieli nadal przyglądać się wszystkim możliwościom dla każdej cząsteczki, ponieważ wiele z nich ma 3, 4, 5 lub więcej asymetrycznych węgli.
Najłatwiej więc określić ilość optycznie czynnych i nieaktywnych izomerów cząsteczki, która ma kilka różne asymetryczne węgle wynikają z wyrażeń matematycznych pokazanych poniżej, które zostały zaproponowane przez Van’t Hoffa i Le Bel:
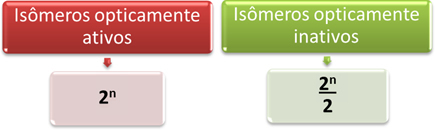
Gdzie „n” to ilość różnych asymetrycznych atomów węgla w cząsteczce. Np. w przypadku aspartamu są to dwa asymetryczne węgle, więc mamy:
- Izomery optycznie czynne: 2Nie = 22 = 4;
- Izomery optycznie nieaktywne: 2Nie = 22 = 2.
2 2
Dało to dokładnie taką kwotę, o której wspomnieliśmy wcześniej.
Co ciekawe, jeden z enancjomerów aspartamu ma słodki smak, który jest używany w sztucznych słodzikach, ale jeden z jego izomerów optycznych ma gorzki smak.
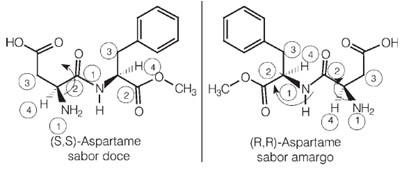
Spójrzmy teraz na inny przykład, cząsteczkę fruktozy:
OH OH OH OH OH OH
│ ║ │ │ │ │
H C ─ C ─ DO ─ DO ─ DO ─ C ─ H
│ │ │ │ │
H
Fruktoza ma trzy asymetryczne atomy węgla, dlatego mamy 8 optycznie czynnych izomerów i 4 optycznie nieaktywnych izomerów, które są 4 mieszaninami racemicznymi.
- Izomery optycznie czynne: 2Nie = 23 = 8;
- Izomery optycznie nieaktywne: 2Nie = 23 = 4.
2 2
Jennifer Fogaça
Absolwent chemii
Źródło: Brazylia Szkoła - https://brasilescola.uol.com.br/quimica/isomeros-moleculas-com-carbonos-assimetricos-diferentes.htm


