Jak sama nazwa wskazuje, między jonami zachodzi wiązanie jonowe. Ponieważ mają przeciwne ładunki, kationy (pierwiastek z ładunkiem dodatnim) i aniony (pierwiastek z ładunkiem ujemnym) przyciągają się elektrostatycznie, tworząc wiązanie. Jednak jonowe ciało stałe to aglomerat kationów i anionów zorganizowanych w ściśle określone kształty geometryczne, zwane sieciami krystalicznymi lub sieciami krystalicznymi.
Na przykład sól (chlorek sodu) powstaje w wyniku ostatecznego przeniesienia elektronu z sodu do chloru, co powoduje powstanie kationu sodu (Na+) i anion chlorkowy (Cl-). W praktyce reakcja ta obejmuje nie tylko dwa atomy, ale ogromną i nieokreśloną liczbę atomów, które tworzą sześcienną sieć krystaliczną, jak pokazano poniżej:
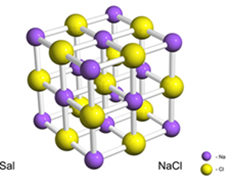
Jeśli spojrzymy na kryształy soli pod skaningowym mikroskopem elektronowym, zobaczymy, że w rzeczywistości są one sześcienne ze względu na ich wewnętrzną strukturę.

Skoro każdy związek jonowy składa się wtedy z nieokreślonej i bardzo dużej liczby jonów, jak możemy przedstawić związek jonowy?
Zwykle stosowana formuła to formuła jednostkowa, który jest tym, który reprezentuje proporcję wyrażoną przez najmniejszą możliwą liczbę kationów i anionów tworzących sieć krystaliczną, tak że całkowity ładunek związku jest zobojętniony. Aby tak się stało, konieczne jest, aby liczba elektronów oddanych przez atom była równa liczbie elektronów otrzymanych przez drugi atom.
Niektóre aspekty dotyczące wzoru jednostkowego związków jonowych są ważne, zobacz niektóre:
- Zawsze najpierw wpisuj kation, a następnie anion;
- Ponieważ każdy związek jonowy jest elektrycznie obojętny, nie ma potrzeby zapisywania poszczególnych ładunków jonowych;
- Liczby w indeksie dolnym pojawiające się po prawej stronie każdego jonu wskazują stosunek atomów kationu do anionu. Liczby te nazywane są indeksami, a cyfra 1 nie jest zapisywana.
Na przykład w przypadku chlorku sodu mamy wzór jednostkowy NaCl, ponieważ na każdy anion chlorkowy przypada dokładnie 1 kation sodu.
Zobacz inny przykład, Al3+ ma trzy ładunki dodatnie, podczas gdy F- ma tylko jeden negatyw, więc do zneutralizowania związku potrzebne są trzy aniony fluorkowe. Zatem wnioskujemy, że jego wzór jednostkowy to AlF3.
Prostym sposobem uzyskania wzoru jednostkowego związku jonowego jest wymiana jego ładunków na jego indeksy, jak pokazano w ogólny sposób poniżej:
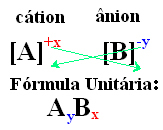
Przykłady:

Innym wzorem używanym do reprezentowania substancji jonowych jest Wzór Lewisa lub formuła elektroniczna, co reprezentuje elektrony z powłoki walencyjnej jonów „kulek” wokół symbolu pierwiastka. W przypadku soli mamy:

Jennifer Fogaça
Absolwent chemii
Źródło: Brazylia Szkoła - https://brasilescola.uol.com.br/quimica/formulas-para-representar-as-ligacoes-ionicas.htm
