Przez długi czas, aż do połowy XIX wieku, odkrywano związki organiczne, a ich nazwy nadawano w zależności od ich pochodzenia. Na przykład kwas mrówkowy po raz pierwszy uzyskano przez destylację czerwonych mrówek; mocznik był uzyskiwany z moczu, kwas mlekowy z mleka i tak dalej.
Jednak z biegiem czasu ilość odkrytych związków organicznych wzrosła i dziś uznaje się, że jest ich ponad 15 milionów. W związku z tym pojawiła się potrzeba sformułowania zasad nomenklatury dla tych związków, które mogłyby być stosowane na arenie międzynarodowej.
Ponadto nomenklatura ta musiałaby osiągnąć dwa cele szczegółowe:
1) Wszystkie związki powinny mieć różne nazwy, aby je odróżnić; nie mogło być dwóch lub więcej związków o tej samej nazwie;
2) Powinna istnieć możliwość nazwania związku według jego wzoru strukturalnego i odwrotnie; to znaczy, biorąc pod uwagę wzór strukturalny, powinno być możliwe dopracowanie jego nazwy.
W 1892 r. na Międzynarodowym Kongresie w Genewie rozpoczęła się dyskusja i racjonalizacja wśród chemików w celu wypracowania nomenklatury, która spełniałaby te cele. Odbyło się wówczas kilka spotkań międzynarodowych, a wreszcie tzw
Nomenklatura IUPAC (Międzynarodowa Unia Chemii Czystej i Stosowanej, akronim wywodzący się z języka angielskiego Międzynarodowa Unia Czystej Chemii Stosowanej). Tym samym organ ten był odpowiedzialny za ustalenie i opracowanie oficjalnych zasad nomenklatury dla wszystkich znanych związków organicznych.Krótko mówiąc, ta nomenklatura składa się z trzech głównych części:
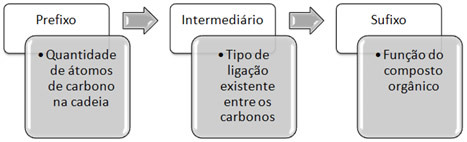
Zauważ, że związki zostały podzielone na funkcje organiczne. Każda rola charakteryzuje się grupą funkcyjną. Na przykład, jeśli związek ma w swojej strukturze tylko węgle i wodory, oznacza to, że należy do grupy węglowodorów. Jeśli masz grupę OH przyłączoną do węgla, stanowi ona alkohol i tak dalej. Związki należące do tej samej grupy mają podobne właściwości.
Poniżej znajduje się tabela określająca terminy najczęściej używane w nomenklaturze związków organicznych:
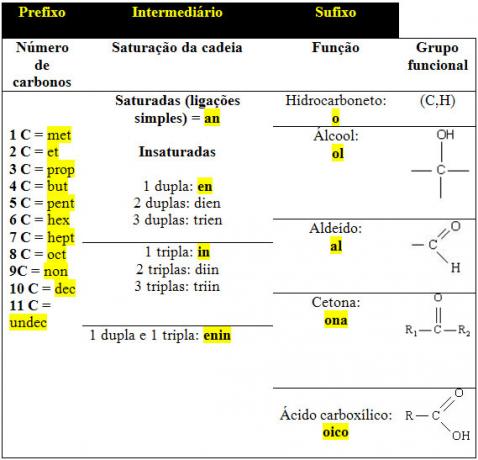
Zobacz kilka przykładów poniżej:
H3CCH3:etan
- Prefiks: ponieważ ma dwa węgle, prefiks to eti;
- Średniozaawansowany: zawiera tylko pojedyncze linki: na;
- Sufiks: ponieważ ma tylko C i H, należy do grupy węglowodorów: O.
O
║
H3CCCH3:propanon
- Prefiks: ma trzy węgle: rekwizyt;
- Pośredni: ma tylko pojedyncze wiązania między węglami: na;
- Przyrostek: ma drugorzędowe wiązanie węglowe z atomem tlenu, a więc pochodzi z grupy ketonowej: łał.
Nomenklatura IUPAC jest uważana za oficjalną nomenklaturę związków organicznych. Nie wyeliminowało to jednak całkowicie innych szczegółowych systemów nazewnictwa, takich jak nazwy przytoczone na początku tego tekstu. Tak więc nazywane są inne formy nomenklatury związków organicznych, które nie są zgodne z zasadami IUPAC zwykłe nomenklatury.
Źródło: Brazylia Szkoła - https://brasilescola.uol.com.br/quimica/nomenclatura-iupac.htm
