O muskowiusz, Liczba atomowa 115, znajdujący się w 15 grupie układu okresowego pierwiastków, jest jednym z ostatnich pierwiastków włączonych do niego w 2015 roku, wraz z pierwiastkami 113, 117 i 118. Jego nazwa jest nawiązaniem do regionu Moskwa, rosyjska stolica.
Moscovium zostało jednak początkowo wyprodukowane w 2003 roku dzięki wspólnej pracy rosyjskich i amerykańskich naukowców. Mimo to, prawie 20 lat po jego wstępnej syntezie, jego podstawowe właściwości wciąż są określane. Tak więc wiele spekuluje się i niewiele wiadomo o jego właściwościach.
Wiedzieć więcej: Nazwy nowych pierwiastków chemicznych — hołd dla miast, regionów i naukowców
abstrakt o moscoviusie
Jest to syntetyczny pierwiastek chemiczny znajdujący się w grupie 15 Układ okresowy.
Po raz pierwszy został zsyntetyzowany w 2003 roku dzięki wspólnej pracy rosyjskich i amerykańskich naukowców.
Stanowi grupę pierwiastków ostatnio włączonych do układu okresowego pierwiastków, w 2015 roku.
Ich badania są bardzo świeże, a podstawowe właściwości wciąż są określane.
Jego produkcja odbywa się za pomocą syntezy jądrowej, przy użyciu 48Ca i atomy 243Jestem.
właściwości Moskwy
Symbol: Mc
Liczba atomowa: 115
Masa atomowa: 288 au.ma (nie oficjalne przez Iupac)
Elektroniczna Konfiguracja: [Rn] 7s2 5f14 6d10 7p3
Najbardziej stabilny izotop: 288Mc (0,159 drugiego okresu półtrwania)
seria chemiczna: grupa 15, pierwiastki superciężkie
Cechy moskiewskie
muskowius jest jeden z ostatnich elementów w komplecieS w układzie okresowym. Jego włączenie miało miejsce 30 grudnia 2015 r., A jego oficjalna nazwa została wydana 8 czerwca 2016 r.
Do tego czasu pierwiastek 115 był znany w języku portugalskim jako ununpentio, od łac. unpentium, którego tłumaczenie brzmi „jeden, jeden, pięć”. Innym przyjętym nazewnictwem był eka-bizmut, co oznacza „podobny do bizmutu”, pierwiastek szóstego okresu grupy 15.
Moskwa jest pierwiastek syntetyczny, co oznacza, że można go wyprodukować tylko w laboratorium. Jest to bardzo powszechne wśród pierwiastków superciężkich, ponieważ ich jądro z wieloma protonami i neutronami nie może się ustabilizować, co uniemożliwia ich znalezienie w naturze.
za bycie niestabilny pierwiastek, on i inne superciężkie pierwiastki prawie natychmiast ulegają rozpadowi radioaktywnemu — emisjom cząstek pierwiastki jądrowe (takie jak cząstki α lub β) — i wynikająca z tego przemiana w inne lżejsze pierwiastki, które mogą być stabilne lub NIE.
Odnośnie do niego należy zauważyć, że jego badania są wciąż bardzo świeże, w końcu mamy do czynienia z elementem wyprodukowanym niecałe 20 lat temu, którego oficjalny status nie ma nawet 10 lat. W związku z tym naukowcy byli bardziej zainteresowani określeniem podstawowych cech, takich jak ich masa atomowa i jego zachowanie chemiczne w niektórych możliwych związkach.
Na przykład najbardziej prawdopodobna masa atomowa wykryta do tej pory dla piżma wynosi 288 atomowych jednostek masy. Nie wspominając o tym, że uzyskanie muscovium jest bardzo skomplikowane, z dochód tylko z jednego atom na dzień.
Ponadto wytworzonego atomu nie zawsze można uchwycić w celu zmierzenia masy. W 2018 roku naukowcy z Berkeley Laboratories w Kalifornii w Stanach Zjednoczonych byli w stanie zmierzyć tylko jedną masę tygodniowo. Zatem, badania nad właściwościami jego związków są nadal w dziedzinie chemii teoretycznej, wraz z obliczeniami i modelami matematycznymi do wyznaczania oczekiwanych rezultatów.
Zdobycie księstwa moskiewskiego
Zdobycie moscovium odbywa się wg Fuzja nuklearna. jony 48Tutaj11+ (Z = 20) przyspieszone uderzenie atomów 243Am (Z = 95), ułożone w postaci AmO2 na okrągłym celu tytan 32 cm², wytwarzając moskow (Z = 115) i trzy neutrony.
Po uderzeniu w około mikrosekundę (10-6 drugi), atom piżma uderza w detektor, który znajduje się około czterech metrów od miejsca zderzenia. Na tej ścieżce pierwiastek przechodzi również przez separator, dzięki czemu lżejsze produkty reakcji są kierowane. W detektorze muscovium jest wykrywany przez jego wzór rozpadu radioaktywnego.
Moscovium, jako atom radioaktywny, ulega rozpadowi alfa (cząstka radioaktywna z dwoma protonami i dwoma neutronami), tworząc w ten sposób pierwiastek 113 (nihonium, Nh) do pierwiastka 105 (dubnium, DB). Wreszcie Db zamienia się w rutherfordium (Rf), który szybko dzieli się na dwa fragmenty. Wzór rozpadu moskovium pokazano poniżej.
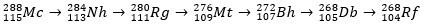
historia Moskwy
muskowiusz był po raz pierwszy zsyntetyzowany w 2003 roku, między 14 lipca a 10 sierpnia, dzięki wspólnej pracy naukowców ze Joint Institute Badań Jądrowych w Dubnej w Rosji oraz Lawrence Livermore National Laboratory w Livermore, Kalifornia.
jony 48Ca, aby mogły zderzać się z atomami 243Am, początkowo produkujący izotop 291Mc. Podczas tego procesu rdzeń nagrzał się do niewiarygodnej 4 x 1011 K, a następnie schłodzony przez bardzo szybką emisję trzech neutronów i promieni gamma.

To działanie utworzyło izotop 288Mc. potem Moskwy został wykryty i przeanalizowany na podstawie jego wzorca rozpadów radioaktywnych (rozpady alfa). Nazwa Moskwa jest hołdem dla regionu moskiewskiego, Rosja.
Przeczytaj też:Seaborgium — syntetyczny pierwiastek chemiczny nazwany na cześć naukowca Glenna Seaborga
Rozwiązane ćwiczenia na muscovius
Pytanie 1
Moskow, niedawno odkryty pierwiastek, został umieszczony w 15 grupie układu okresowego pierwiastków. Na podstawie innych pierwiastków z tej grupy oczekiwany wodorek dla tego pierwiastka to:
A) McH
B) McH2
C) McH3
D) McH4
E) Mc2H3
Rezolucja:
Alternatywa C
Inne elementy grupy 15, takie jak azot To jest fosfor, przedstaw wzory NH3 i pH3 po związaniu z wodorem. Oczekuje się zatem, że moscovium przedstawia wzór McH3 Również.
pytanie 2
W 2003 roku dzięki wspólnej pracy rosyjskich i amerykańskich naukowców po raz pierwszy zsyntetyzowano moskovium (Z = 115). W tym czasie izotop 288Wykryto Mc, a jego produkcja była niezbędna do umieszczenia tego pierwiastka w układzie okresowym. Liczba neutronów w tym izotopie wynosi:
115
B) 288
C) 403
D) 173
E) 170
Rezolucja:
Alternatywa D
Liczba neutrony można obliczyć w ten sposób:
A = Z + n
Gdzie A to liczba masowa, Z to liczba atomowa, a n to liczba neutronów. Podstawiając wartości, otrzymujemy:
288 = 115 + rz
n = 288 – 115
n = 173
Stefano Araujo Novais
Nauczyciel chemii