Poznaj Yarę! Sztuczna inteligencja Brasil Escola! Poprawia eseje w standardzie Enem i szybko i bezpłatnie odpowiada na pytania z różnych dziedzin!
A nazewnictwo węglowodorów charakteryzuje się głównie obecnością przyrostka „-o”. Takie zasady nomenklatury są określone przez Międzynarodową Unię Chemii Czystej i Stosowanej w książce popularnie znanej jako „Niebieska księga”.
Węglowodory (organiczna funkcja, która ma w swojej strukturze tylko węgiel i wodór), jednak różnią się wrostkiem, ponieważ mogą być nasycone (jak alkany i cykloalkany) i nienasycone (jak alkeny, alkiny i cykloalkeny). Związki aromatyczne (takie jak benzen) również mają specyficzny system nazewnictwa, niewiele różniący się jednak od łańcuchów zamkniętych.
Przeczytaj też: Jak poznać nazewnictwo związków o funkcjach mieszanych?
Tematyka tego artykułu
- 1 - Podsumowanie nomenklatury węglowodorów
- 2 - Lekcja wideo dotycząca nazewnictwa węglowodorów
- 3 - Jaka jest zasada nazewnictwa węglowodorów?
- 4 - Nazewnictwo alkanów
- 5 - Nazewnictwo alkenów
- 6 - Nazewnictwo alkadienów
- 7 - Nazewnictwo alkinów
- 8 - Nazewnictwo cykloalkanów
- 9 - Nazewnictwo cykloalkenów
- 10 - Nomenklatura aromatów
- 11 - Rozwiązane ćwiczenia z nomenklatury węglowodorów
Podsumowanie nomenklatury węglowodorów
Wszystkie węglowodory mają przyrostek „-o”.
Zasady nazewnictwa określa Międzynarodowa Unia Chemii Czystej i Stosowanej, IUPAC.
Chociaż nie różnią się sufiksem, węglowodory będą się różnić wrostkiem, będąc „-an-” dla tych, które mają nasycony łańcuch, „-en-” dla tych z podwójnym wiązaniem i „-in” dla tych z podwójnym wiązaniem potroić.
Aromaty, takie jak benzen, mają swój własny system nazewnictwa, trochę inny niż pozostałe. węglowodory, jednak z podobieństwami w stosunku do systemu nazewnictwa związków łańcuchowych Zamknięte.
Lekcja wideo na temat nazewnictwa węglowodorów
Jaka jest zasada nazewnictwa węglowodorów?
Węglowodory, a także wszystkie inne związki chemii organicznej, mają swoje oficjalne (lub systematyczne) nazwy określone przez IUPAC (w języku portugalskim, Międzynarodowa Unia Chemii).
Przepisy te są okresowo aktualizowane i są zawarte w książce Nomenklatura chemii organicznej: zalecenia IUPAC i preferowane nazwy, którego wolnym tłumaczeniem może być Organic Chemistry Nomenclature: IUPAC Recommendations and Preferred Names. Taka książka jest powszechnie nazywana „Niebieską Księgą” IUPAC.
Węglowodory, zgodnie z obowiązującymi przepisami, zawsze musi mieć przyrostek „-o”.
Teraz nie przestawaj... Po reklamie jest więcej ;)
nazewnictwo alkanów
alkany są węglowodorami, które mają otwarty i nasycony łańcuch. W konsekwencji, mają, oprócz przyrostka „-o” węglowodorów, przedrostek „-an-”, wskazując tylko pojedyncze wiązania między atomami węgla.
Przykłady:
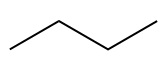
Przedrostek „but-” jest używany do wskazania 4 atomów węgla w łańcuchu.
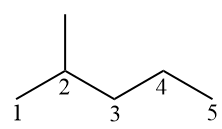
Jeśli w alkanie są rozgałęzienia, muszą one mieć jak najmniej rozgałęzień.. Zatem główny łańcuch (pentan) musi zaczynać swoją numerację od skrajnego lewego końca, tak aby metyl miał najniższą możliwą liczbę (2).
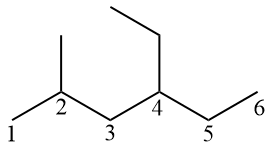
Główny łańcuch musi być ponumerowany od lewej do prawej, tak aby gałęzie znajdowały się na atomach węgla 2 i 4. Gdyby numerować od prawej do lewej, gałęzie byłyby na węglach 3 i 5, które byłyby dłuższe.
Chociaż metyl otrzymuje najniższą liczbę, w oficjalnej nomenklaturze gałęzie (lub rodniki) muszą być ułożone w porządku alfabetycznym. Dlatego etyl (który zaczyna się na literę E) występuje przed metylem (który zaczyna się na literę M). W języku portugalskim myślnik musi być używany przed słowami zaczynającymi się na literę H. Dlatego używamy łącznika w „metyloheksanie”, ale nie w „metylopentanie”.
Zobacz też: Jaka jest nomenklatura alkanów zawierających więcej niż dziesięć atomów węgla?
nazewnictwo alkenów
alkeny to węglowodory, które również mają otwarty łańcuch, ale mają podwójne wiązanie między atomami węgla, co czyni je nienasyconymi. Powoduje to zmianę nazwy w stosunku do alkanów, czyli tzw zastąpienie wrostka „-an-” alkanów przez „-en-”. Ponadto, według Iupaca, wiązania podwójne również muszą być ponumerowane. Wiązania podwójne również powinno być jak najmniej i mieć pierwszeństwo przed rozgałęzieniami.
Przykłady:
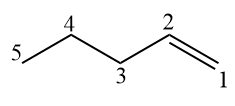
Dla alkenów zawierających więcej niż 3 atomy węgla, podwójne wiązanie musi być ponumerowane obok wrostka „-en-”. w oficjalnej nazwie.
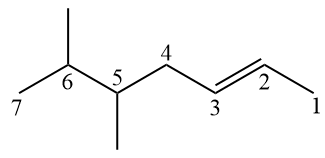
Pomiędzy rozgałęzieniem a wiązaniem podwójnym pierwszeństwo ma wiązanie podwójne, aby było ich jak najmniej.
nazewnictwo alkadienów
Alkadieny to węglowodory, które mają dwa wiązania podwójne. Wrostek pozostaje „-en-”, ale z dodanie deskryptora numerycznego „di-” przed „-en-”, aby wskazać, że istnieją dwa wiązania podwójne. Pod względem fonetycznym, po przedrostku ciągu głównego dodaje się literę „a”.
Przykład:
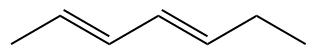
nazewnictwo alkinów
alkiny są węglowodorami, które mają takie same właściwości jak alkeny, z tą różnicą, że zamiast podwójnego mają wiązanie potrójne. To również przynosi różnicę w wrostku, z zamiana wrostka „-en-” na „-in-”.
Przykłady:
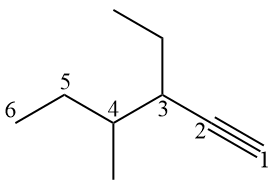
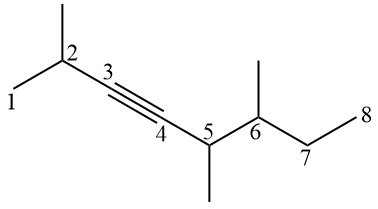
Ponieważ węgiel sp ma geometrię liniową, często przedstawia się alkin o geometrii liniowej w wiązaniu potrójnym, co utrudnia początkowo policzenie węgli. Chodzi o to, aby zwizualizować wiązania π, które ograniczają obecne tam atomy węgla.
Nazewnictwo cykloalkanów
Cykloalkany to węglowodory o zamkniętym łańcuchu i nasycone. Dlatego w swojej oficjalnej nazwie będzie miał przedrostek „ciclo-” przed nazwą głównego łańcucha, a także infiks „-an-”, tradycyjne łańcuchy nasycone.
Przykłady:

Jednopodstawione cykloalkany (z rozgałęzieniem) nie mogą mieć numeracji rozgałęzienia w oficjalnej nazwie, gdyż jest ona zbędna (przecież rozgałęzienie musi być na pozycji 1).
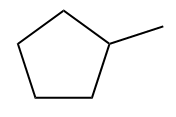
Jednakże, jeśli istnieją więcej niż dwa oddziały, muszą one być ponumerowane normalnie w oficjalnej nazwie, z numerem 1 nadanym priorytetem w porządku alfabetycznym. Następnie numeracja musi obracać się zgodnie z ruchem wskazówek zegara lub przeciwnie do ruchu wskazówek zegara, tak aby pozostałe gałęzie miały jak najniższy numer.
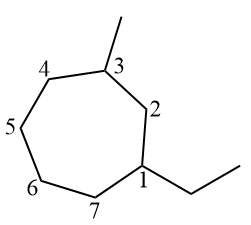
Zauważ, że gałąź etylowa ma numer 1, ponieważ litera E występuje przed literą M oznaczającą metyl w alfabecie. Następnie numeracja cyklu została obrócona w kierunku przeciwnym do ruchu wskazówek zegara, tak aby gałąź metylowa miała najniższą możliwą liczbę (3).
Nazewnictwo cykloalkenów
Cykloalkeny to węglowodory, które mają nienasycony łańcuch i dlatego mieć wrostek „-en-”. Będąc rozgałęzionymi, pierwszeństwo będzie miało nienasycenie, podobnie jak alkeny.
Przykłady:
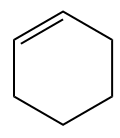
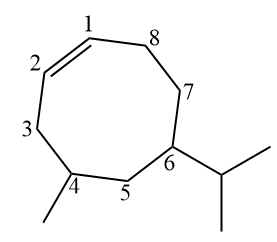
W przypadku poprzedniej struktury rozgałęzionej węgle 1 i 2 zawsze będą atomami węgla podwójnego, ale będą ponumerowane tak, aby rozgałęzienia miały jak najmniejszą liczbę. Jednak izopropyl wyprzedza metyl pod względem porządku alfabetycznego i dlatego jest zapisywany jako pierwszy (I pojawia się przed M).
Nomenklatura aromatów
Węglowodory aromatyczne mają struktury, które obowiązkowo mają cykle lub cykle heksagonalne zawierające trzy naprzemienne wiązania podwójne. W szkole średniej zachowuje się znaczną część badań nad węglowodorami aromatycznymi benzen (C6H6). Benzen jest zgodny z zaleceniami IUPAC dla węglowodorów o zamkniętym łańcuchu, ale nazwa „benzen” jest akceptowana dla głównego łańcucha.
W przypadku dipodstawionych związków benzenu firma Iupac oficjalnie nie zaleca już używania deskryptorów lokalizacji orto (o), meta (m) i para (p), jednak takie lokalizatory są nadal szeroko stosowane w testach i konkursach i dlatego będą cytowane Tutaj.
Przykłady:

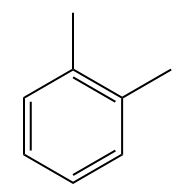
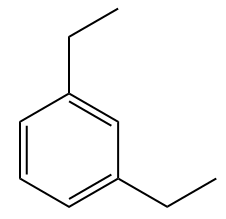
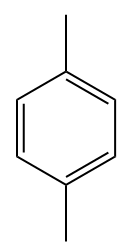
Naftalen, który składa się z dwóch skondensowanych pierścieni benzenowych, ma stałą liczbę, zgodnie z IUPAC:
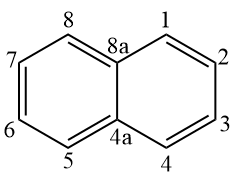
Dlatego następującą strukturę należy nazwać zgodnie z ustaloną numeracją.
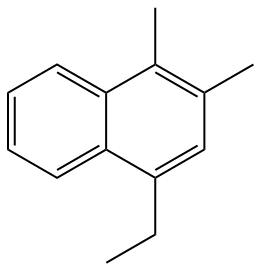
Wiedz także: Jakie są główne funkcje organiczne?
Rozwiązane ćwiczenia z nomenklatury węglowodorów
Pytanie 1
(IME) Izopren jest toksycznym związkiem organicznym stosowanym jako monomer do syntezy elastomerów w reakcjach polimeryzacji. Biorąc pod uwagę strukturę izoprenu, jaka jest jego nomenklatura Iupac?

A) 1,3-buten
B) 2-metylobutadien
C) 2-metylobuten
D) pentadien
E) 3-metylo-butadien
Rezolucja:
Alternatywa B.
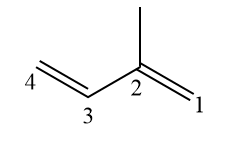
Numeracja struktury jest przedstawiona na poprzednim obrazie. Przy rozgałęzieniu przy węglu 2 (rozgałęzienia powinny mieć najmniejszą możliwą liczbę), nienasycenie może występować tylko przy atomach węgla 1 i 3, bez innej możliwej pozycji. Dlatego są one pomijane w oficjalnej nazwie, ponieważ zbędne jest mówienie buta-1,3-dien.
Dlatego nazwa pozostaje 2-metylobutadienem.
pytanie 2
(UEG) Poniższy węglowodór, zgodnie z regułami nomenklatury IUPAC (Międzynarodowej Unii Chemii Czystej i Stosowanej), jest
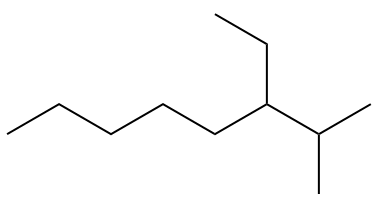
A) 3-etylo-2-metylooktan.
B) 6-etylo-7-metylooktan.
C) 3-izopropyloktan.
D) 2-metylo-3-etylooktan.
Rezolucja:
Alternatywa A.
Zwróć uwagę na numerację danego węglowodoru na poniższym obrazku.
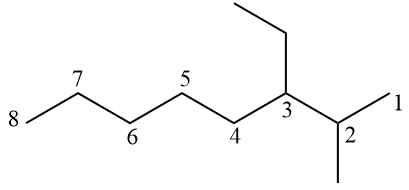
Gałęzi powinno być jak najmniej, więc numeracja zaczyna się od skrajnej prawej strony. Pisząc oficjalną nazwę, gałęzie należy umieścić w kolejności alfabetycznej: 3-etylo-2-metylooktan.
Źródło
FAVRE, H. A.; POWELL, W. H.; MOS, G. P. Nomenklatura chemii organicznej. Zalecenia IUPAC i preferowane nazwy 2013. Londyn: Królewskie Towarzystwo Chemii, 2013.
Stefano Araujo Novais
Nauczyciel chemii
Tutaj w tym tekście znajdziesz definicję grupy funkcyjnej alkadienów, zobaczysz kilka ich przykładów w życiu codziennym oraz sposób ich nazewnictwa.
Dowiedz się więcej o alkanach, ich właściwościach fizykochemicznych, oficjalnej nomenklaturze, ogólnym wzorze i zastosowaniach. Wykonaj ćwiczenia na ten temat.
Kliknij tutaj, dowiedz się, czym są alkeny, poznaj ich właściwości i charakterystykę oraz poznaj kryteria stosowane w ich oficjalnej nomenklaturze.
Cykloalkany to węglowodory cykliczne i nasycone, to znaczy o łańcuchu zamkniętym i wiązaniach pojedynczych.
Związki aromatyczne, areny, polarność, nierozpuszczalne, rozpuszczalne, niepolarne rozpuszczalniki, eter, tetrachlorek węgla, węglowodory, insektycydy, barwniki, rozpuszczalniki, materiały wybuchowe, rakotwórcze, toluen, metylobenzen, narkotyki, klej szewc.
Dowiedz się więcej o właściwościach, rodzajach, nazewnictwie i miejscach występowania węglowodorów.