TEN izomeria jest to zjawisko obserwowane, gdy różne związki tworzą równe ilości tego samego typu atomów.
W związku z tym możemy znaleźć substancje chemiczne o tym samym wzorze cząsteczkowym i różnych wzorach strukturalnych lub układach przestrzennych.
Zjawisko to jest szeroko obserwowane w chemii organicznej, która bada związki węgla. Ponieważ każdy atom tego pierwiastka może tworzyć 4 wiązania chemiczne, można zaobserwować różne kombinacje.
Ponieważ zmiana układu atomów powoduje powstawanie nowych substancji, w konsekwencji mają one różne właściwości fizyczne i chemiczne.
Kiedy mówimy, które związki są izomery oznacza, że mają równe części, ponieważ słowo to jest połączeniem dwóch terminów pochodzenia greckiego: isos, oznacza "naprawdę" i sam, czyli „części”.
Dwie główne grupy izomerii to płaszczyzna i przestrzeń (stereoizomeria).
TEN płaska izomeria można to zobrazować za pomocą płaskiego wzoru strukturalnego związków i ma pięć klas: pozycję, funkcję, łańcuch, kompensację i tautomery.
TEN
izomeria kosmiczna obserwuje się ją na podstawie orientacji związków i dzieli się na geometryczną (cis-trans) i optyczną.Pojęcie izomerii zostało wprowadzone w 1830 roku przez szwedzkiego naukowca Jacoba Berzeliusa.
Przykłady izomerów
TEN izomeria łańcuchowa występuje, gdy ten sam zestaw atomów łączy się, tworząc struktury tej samej grupy funkcyjnej, ale o różnych łańcuchach.
Przykład: wzór cząsteczkowy C4h10 węglowodoru może być prosty lub rozgałęziony.

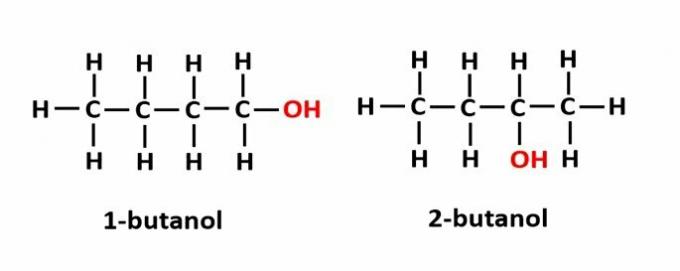
TEN izomeria pozycji występuje, gdy związki są tworzone przez te same grupy funkcyjne, ale znajdują się w różnych pozycjach łańcucha.
Przykład: wzór cząsteczkowy C4h9OH odpowiada dwóm rodzajom alkoholu.
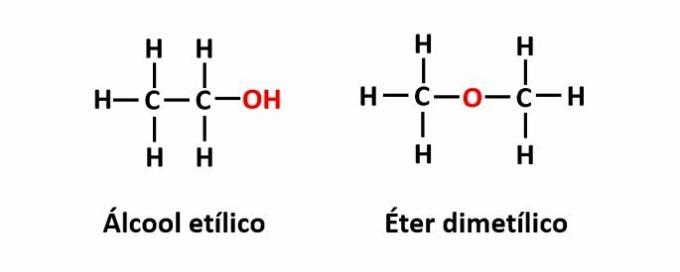
TEN izomeria funkcji występuje, gdy ten sam wzór cząsteczkowy odpowiada dwóm związkom z różnymi grupami funkcyjnymi.
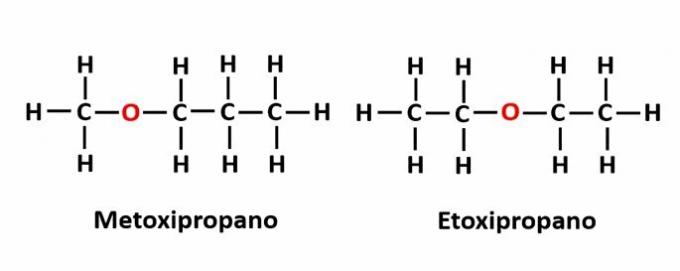
Przykład: wzór cząsteczkowy C2h6O odpowiada dwóm izomerom, które mają funkcje alkoholu (-OH) i eteru (-O-).
TEN izomeria kompensacyjna występuje, gdy w łańcuchu znajduje się heteroatom i zajmuje różne pozycje. Jest to szczególny przypadek izomerii pozycyjnej.
Przykład: wzór cząsteczkowy C4h10Wskazuje na obecność atomu tlenu w łańcuchu, ale jego pozycja może się zmieniać i tworzyć różne związki.
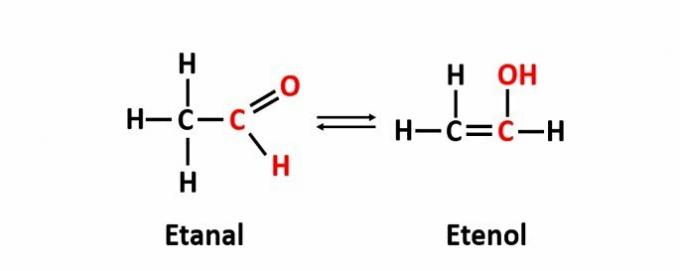
TEN izomeria dynamiczna, zwany również tautomery, występuje, gdy dwa związki o różnych funkcjach znajdują się w tym samym roztworze w równowadze dynamicznej. Jest to szczególny przypadek izomerii funkcji.
Przykład: wzór cząsteczkowy C2h4O odpowiada związkom z funkcjami aldehydowymi i enolowymi.
Dowiedz się więcej o płaska izomeria.
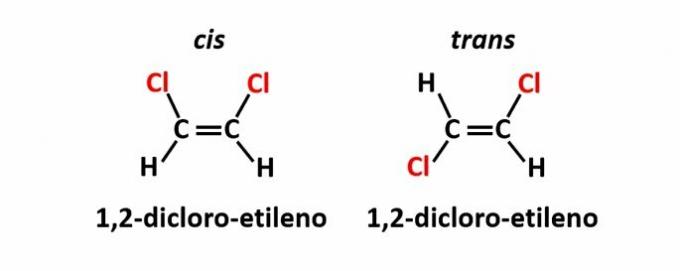
TEN izomeria geometryczna, zwany także izomerią cis-trans, występuje, gdy obecność podwójnego wiązania lub struktury cyklicznej powoduje, że równe ligandy znajdują się po tej samej stronie płaszczyzny (cis) lub po przeciwnych stronach (trans).
Przykład: atomy chloru w związkach o wzorze cząsteczkowym C2h2Cl2 mogą mieć dwie struktury przestrzenne.
TEN izomeria optyczna występuje, gdy podczas odchylania spolaryzowanego światła emitowanego na konstrukcję związki potrafią odchylić wiązkę świecący w lewo, jeśli jest to izomer lewoskrętny (l), lub w prawo, gdy jest to izomer prawoskrętny (D).
Przykład: Ten rodzaj izomerii występuje w przypadku kwasu mlekowego. Należy zauważyć, że obrazy spektralne izomerów nie nakładają się, dlatego nazywa się je enancjomerami.
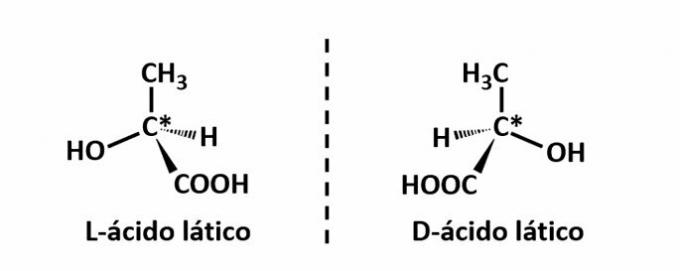
Symbol C* wskazuje na obecność chiralnego węgla w tej strukturze, tj. atomu węgla z 4 różnymi łącznikami.
Dowiedz się więcej o izomerii z treścią:
- Rodzaje izomerii
- izomer kosmiczny
- izomer geometryczny
- izomer optyczny
- Ćwiczenia z izomerii płaskiej