Reakcje dodatek są ważnymi działaniami w odniesieniu do syntez organicznych, ponieważ dzięki nim można opracować ciekawą liczbę substancji organicznych.
Aby zaszła reakcja addycji, konieczne jest utworzenie dwóch miejsc wiążących w łańcuchu węglowym, co następuje po prostu, gdy łańcuch jest nienasycony (obecność pi link). Tak więc, gdy łącze pi jest zerwane, witryny pojawiają się w łańcuchu.
Grupa substancji, które mogą być stosowane w syntezach dodatkowych to: cykloalkany lub cyklany, grupa węglowodorów o łańcuchach cyklicznych i nasyconych. Wymykają się ogólnej zasadzie dodawania, ponieważ nie mają łącza pi, ale w zależności od pewnych warunków (ciepło, metal katalizatora, kwaśne medium) mogą przejść przerwanie łańcucha między dwoma atomami węgla, powodując pojawienie się dwóch miejsc wiązania, aby nastąpiło dodanie. Istnieje jednak fakt, który ogranicza stosowanie tych związków. Faktem jest wezwanie teoria naprężeń pierścieniowych, zaproponowana przez Adolfa V. Bayer w 1885 r..
Aby wiązanie sigma między węglami zostało zerwane, musi istnieć pewna niestabilność między węglami. Ta niestabilność jest związana z kątem wiązań między węglami. Według Bayera kąt, który zapewnia a
świetna stabilność dla łącza sigma to 109,47O. Zatem łańcuchy, które mają kąt między węglami mniejszy niż 109,47O mają tendencję do niestabilności w wiązaniach sigma między węglami tworzącymi łańcuchy, co sprzyja ich pękaniu w połączeniu z idealnymi warunkami zewnętrznymi.Jedyne cykloalkany, które mają kąt mniejszy niż 109,47O wśród jego węgli są cyklopropan (60O), cyklobutan (90O) i cyklopentan (108O). Cyklopentan ma kąt bardzo bliski 109,47O ma bardzo stabilne wiązania sigma, dlatego nie może ulegać żadnej reakcji addycji. Poniżej mamy struktury tych trzech cykloalkanów:

Wzór strukturalny odpowiednio cyklopropanu, cyklobutanu i cyklopentanu
Obserwacja: Każdy cykloalkan, który ma więcej niż 5 atomów węgla w łańcuchu, przeprowadzi reakcję podstawienia dla przykład, a nigdy dodatek, ponieważ wiązania sigma między ich atomami węgla są niezwykle stabilny.
Reakcje addycji, które mogą zachodzić w przypadku cykloalkanów, są w zasadzie wszystkie, ale w przypadku cyklopentanu mogą one podlegać tylko uwodornieniu i halogenowaniu. Poniżej przykłady dodatków z cykloalkanami i warunki ich występowania:
a) Uwodornianie
Reakcja cykloalkanu z cząsteczką wodoru w obecności sproszkowanego katalizatora metalicznego (cynk, nikiel lub platyna) w obecności ogrzewania (około 180°COC). W tej reakcji cykloalkan spowoduje powstanie a alkany. W tej reakcji, po przerwaniu cyklu, jeden atom wodoru jest dodawany do każdego węgla wiązania sigma, które zostało zerwane.

Reakcja addycji w cyklobutanie z użyciem wodoru
b) Halogenacja
Reakcja cykloalkanu z cząsteczką halogenu (na przykład chlor, brom, jod) w obecności katalizatora chlorku żelaza III (FeCl3). W tej reakcji cykloalkan spowoduje powstanie a halogenek organiczny z dwoma atomami halogenu w łańcuchu. Po zerwaniu cyklu mamy dodanie atomu halogenu na każdym z węgli zerwanego wiązania sigma.

Reakcja addycji w cyklobutanie z użyciem bromu
c) Reakcja z halogenowodorkami (halogenki kwasowe)
Reakcja cykloalkanu z cząsteczką nieorganicznego hydratu zawierającego halogen (HCl. HBr, HI). Ponieważ jako reagent stosuje się kwas, nie stosuje się katalizatora. W tej reakcji cykloalkan spowoduje powstanie a halogenek organiczny z tylko jednym atomem halogenu w łańcuchu. Po zerwaniu cyklu mamy dodanie atomu wodoru na jednym z węgli zerwanego wiązania sigma i halogenu na drugim węglu. Przestrzeganie zasady Markownikowa (H na najbardziej uwodornionym węglu i halogen na najmniej uwodornionym węglu).
Uwaga: Występuje tylko w przypadku cyklopropanu i cyklobutanu.
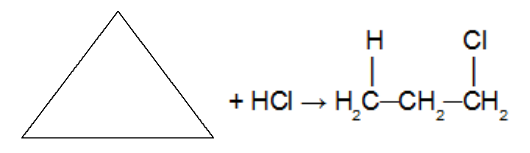
Reakcja addycji w cyklopropan z użyciem kwasu solnego
Uwaga: Występuje tylko w przypadku cyklopropanu i cyklobutanu.
d) Nawodnienie
Reakcja cykloalkanu z cząsteczką wody w obecności kwasu siarkowego i ogrzewania. W tej reakcji cykloalkan spowoduje powstanie a monoalkohol (alkohol z tylko jedną grupą OH w łańcuchu). Po zerwaniu cyklu mamy dodanie atomu wodoru na jednym z węgli zerwanego wiązania sigma i hydroksylu (OH) na drugim węglu. Przestrzeganie reguły Markownikowa (H na najbardziej uwodornionym węglu i hydroksyl na najmniej uwodornionym węglu).
Uwaga: Występuje tylko w przypadku cyklopropanu i cyklobutanu.

Reakcja addycji w cyklopropan z użyciem kwasu solnego
Przeze mnie Diogo Lopes Dias
Źródło: Brazylia Szkoła - https://brasilescola.uol.com.br/quimica/adicoes-ciclanos.htm
