Kp jest akronimem używanym do określenia stała równowagi pod względem ciśnień cząstkowych. Ta stała działa na przykład z wartościami gazowych uczestników równowagi w jednostce ATM.

Równanie przedstawiające reakcję chemiczną ze składnikami gazowymi
W tym równaniu wszyscy uczestnicy są w stanie gazowym, więc gdy uczestniczący gaz ma ciśnienie cząstkowe w mieszaninie, jest reprezentowany przez skrót pX.
Przy ustalaniu równania równowagi chemicznej (w kategoriach stężenia) produkty należy umieścić w liczniku, a reagenty w mianowniku:
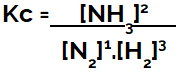
Wyrażanie Kc równowagi tworzenia amoniaku
wyrażenie stała równowagi pod względem ciśnienia (Kp) podąża za wzorcem Kc, to znaczy ciśnienia cząstkowe odczynników są umieszczone w mianowniku, a ciśnienia cząstkowe produktów w liczniku:
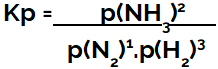
Wyrażanie Kp równowagi tworzenia amoniaku
Obserwacja: Jeśli równanie reakcji bilans chemiczny nie przedstawiaj żadnego uczestnika gazowego, nie pojawi się automatycznie Kp.
Przykład: (PUC-MG) Do reakcji: 2 CO(g) + O2(g)? 2 CO2(g), ciśnienia cząstkowe CO
(g) to jest2(g) w stanie równowagi wynoszą one odpowiednio 0,2 atm i 0,4 atm. Całkowite ciśnienie w układzie wynosi 1,4 atm. Wartość Kp dla reakcji jest:a) 56,2
b) 40,0
c) 35,6
d) 28,4
e) 25,6
Dane dostarczane przez ćwiczenie to:
ciśnienie cząstkowe tlenku węgla (pCO) = 0,2 atm;
Ciśnienie cząstkowe tlenku węgla (pO2) = 0,4 atm;
Ciśnienie całkowite = 1,4 atm;
Aby określić Kp tego układu, musimy wykonać następujące kroki:
Krok 1: Wyznacz ciśnienie cząstkowe tlenku węgla (pCO2).
W tym celu pamiętaj tylko, że ciśnienie całkowite (pt) jest sumą wszystkich ciśnień cząstkowych:
pt = pCO + pCO2 + pO2
1,4 = 0,2 + p (CO2) + 0,4
1,4 - 0,2 - 0,4 = pCO2
pCO2 = 0,8 atm
Drugi krok: Określ Kp ćwiczenia.
W tym celu wystarczy użyć wartości w wyrażeniu stałej równowagi Kp:
Kp = (pCO2)2
(pCO)2.(pył2)1
Kp = (0,8)2
(0,2)2.(0,4)1
Kp = 0,64
0,04.0,4
Kp = 0,64
0,016
Kp = 40 atm-1
Przeze mnie Diogo Lopes Dias
Źródło: Brazylia Szkoła - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-kp.htm

