Cząsteczka to zbiór takich samych lub różnych atomów połączonych wiązaniami kowalencyjnymi.
Te związki chemiczne są elektrycznie obojętne i stanowią jednostkę tworzącą substancję.
Istnieją proste cząsteczki, takie jak tlen (O2) powietrza, którym oddychamy. Istnieją jednak również związki złożone, takie jak buckyballs (60 atomów węgla połączonych w kulisty kształt), które są największymi cząsteczkami, jakie kiedykolwiek znaleziono w kosmosie.
Badanie molekuł
Wiązanie kowalencyjne w cząsteczce odpowiada współdzieleniu elektronów, zwykle między pierwiastkami niemetalicznymi.
Zobacz cząsteczkę wody jako przykład prostego związku.
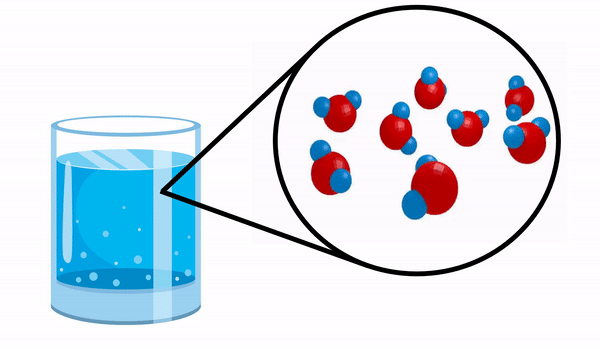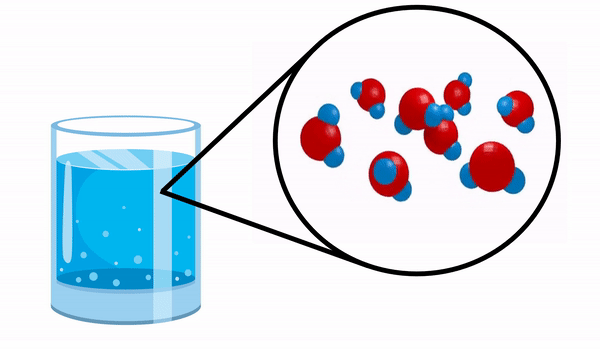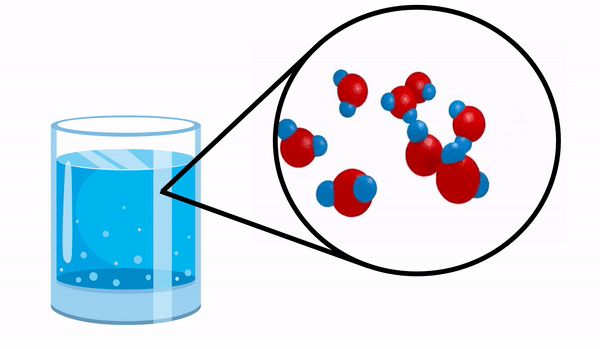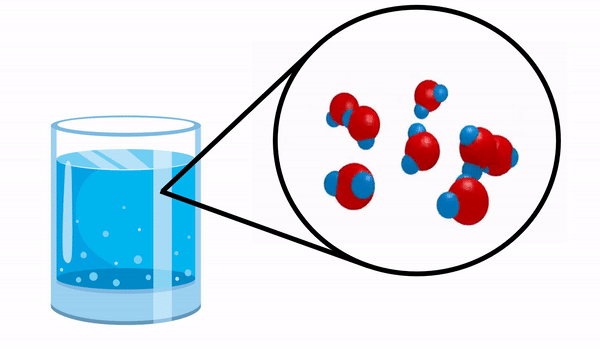
Kiedy obserwujemy szklankę z woda nie mamy pojęcia, że ta substancja składa się z kilku cząsteczek H2O. Ten wzór wskazuje, że woda składa się z 3 atomów: dwóch atomów wodoru i jednego tlenu, które dzielą ze sobą elektrony.
Cukier, którego używamy do słodzenia soków i robienia ciast, również składa się z cząsteczek. Jednostką tworzącą cukier jest sacharoza.

Ta cząsteczka jest znacznie bardziej złożona, ponieważ jest 45 atomy połączony. Tworzą go: 12 atomów węgla, 22 atomy wodoru i 11 atomów tlenu.
Cząsteczki to struktury o znanej masie cząsteczkowej, ale są też makrocząsteczki, które są „gigantycznymi strukturami” złożonymi z tak wielu atomów, że ich skład jest nawet nieokreślony. Przykładem tego typu jest diament, makrocząsteczka zbudowana z wielu atomów węgiel w sieci kowalencyjnej.
Wiązanie kowalencyjne
Pomiędzy dwoma atomami powstaje kowalencyjne wiązanie chemiczne, gdy dzielą one swoje elektrony bardziej zewnętrzne (wartościowości). Cząsteczki mogą mieć dwa rodzaje wiązań:
Molekularne wiązanie kowalencyjne: para elektronów dwóch atomów wiążących jest wspólna.

Wiązanie kowalencyjne (celownik): wspólne elektrony pochodzą tylko z jednego z zaangażowanych atomów.
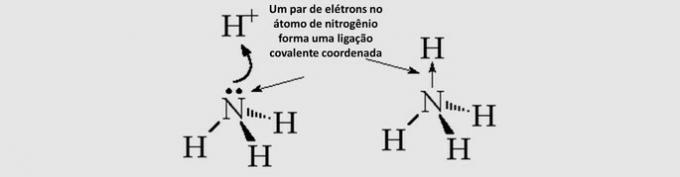
Geometria molekularna
Kiedy powstaje cząsteczka, atomy są rozmieszczone w różny sposób, dzięki czemu układ przestrzenny jest bardziej stabilny. Dlatego kompozyty mają różne geometrie.
Oto niektóre z geometrii, jakie mogą mieć cząsteczki.
| Geometria molekularna | ||
|---|---|---|
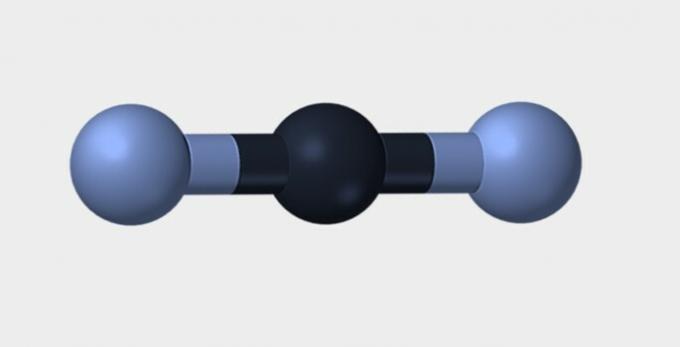
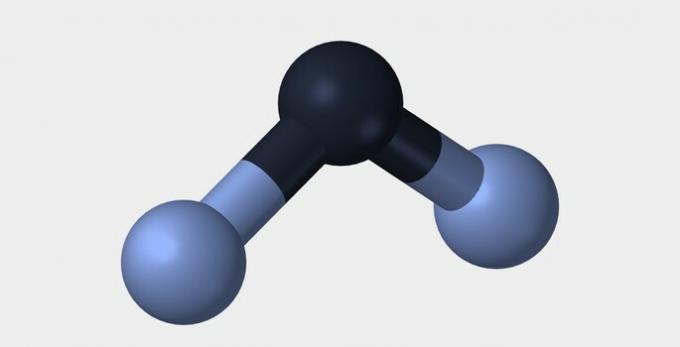
| Liniowy | Kątowy | Trójkątny |
 |
 |
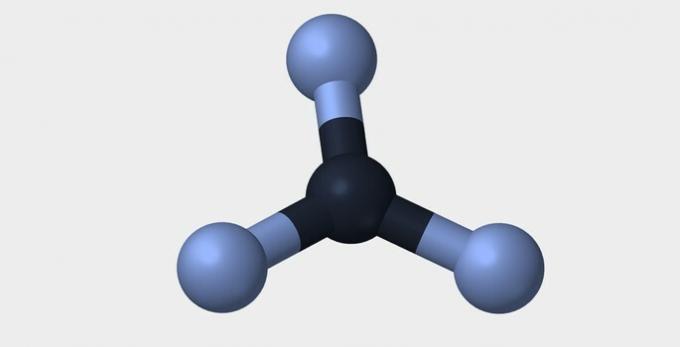 |
| Piramidalny | czworościenny | ośmiościenny |
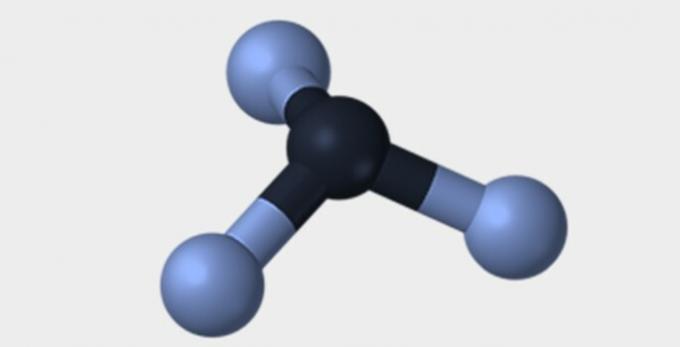 |
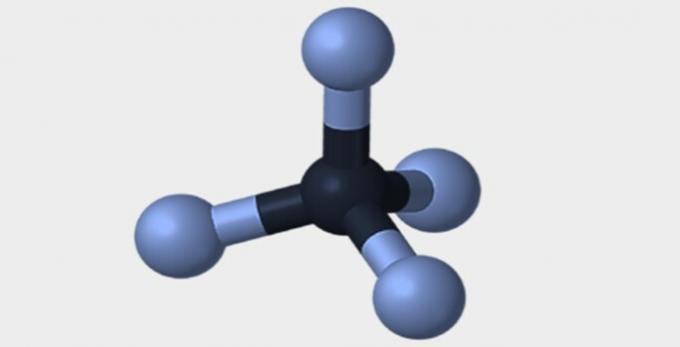 |
 |
Cząsteczki polarne i niepolarne
Cząsteczki są klasyfikowane według biegunowość.
cząsteczki niepolarne: nie ma różnicy w elektroujemności między atomami.
| Azot (N2) | dwutlenek węgla (CO2) |
|---|---|
 |
 |
Azot (N2) jest cząsteczką niepolarną, ponieważ jest przez nią utworzona pierwiastek chemiczny a zatem nie ma różnicy w elektroujemności. dwutlenek węgla (CO2) jest niepolarny ze względu na swoją liniową geometrię, która stabilizuje przyciąganie tlenu przez elektrony.
cząsteczki polarne: istnieje różnica w elektroujemności między atomami, z biegunem dodatnim i biegunem ujemnym.
| Woda (H2O) | Amoniak (NH3) |
|---|---|
 |
 |
W obu przykładach widzimy, że centralne atomy tlenu i azotu mają niesparowane pary elektronów, które tworzą chmury elektronowe. Ponieważ wokół centralnych atomów jest więcej chmur elektronowych niż ustalonych wiązań chemicznych, cząsteczki są polarne.
Przykłady cząsteczek
| Substancja | funkcje | Cząsteczka | Formuła |
|---|---|---|---|
| Wodór | Paliwo i obfitość w skorupę ziemską. | 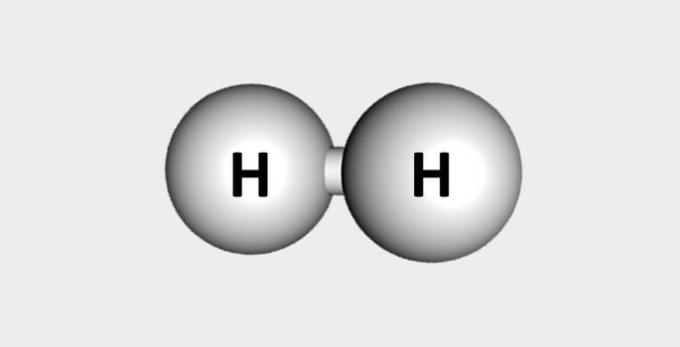 |
H2 |
| Tlen | Niezbędny do oddychania i uczestniczy w różnych reakcjach chemicznych | 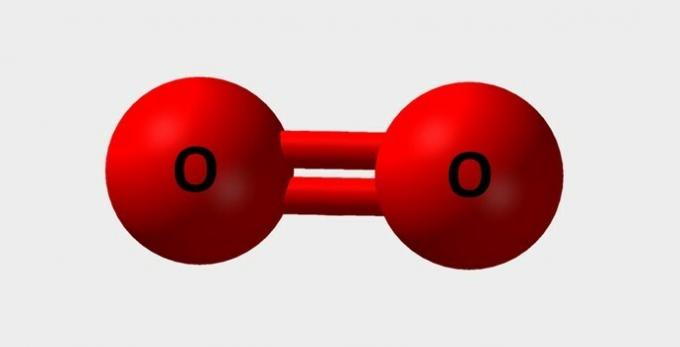 |
O2 |
| Siarka | Żółty proszek używany do produkcji barwników. | 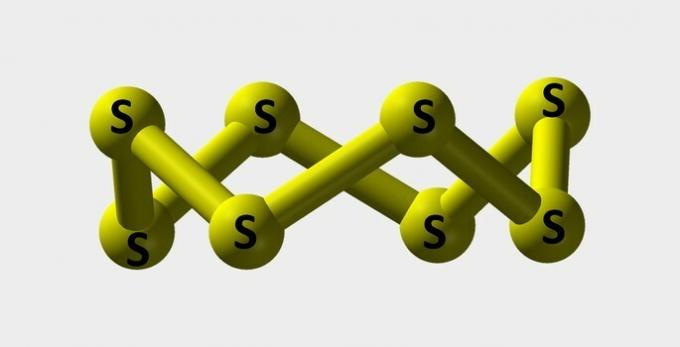 |
s8 |
| Dwutlenek węgla | Stosowany w gaśnicach i czynnikach chłodniczych. | 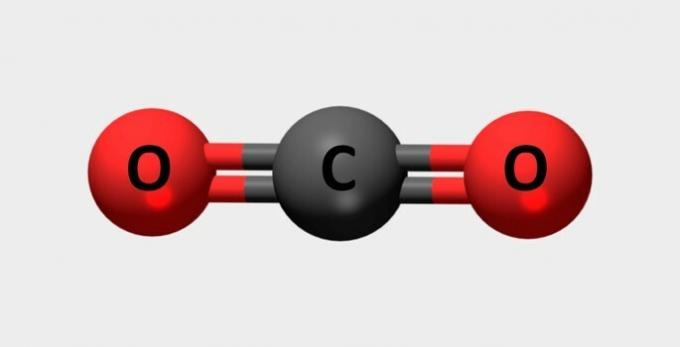 |
WSPÓŁ2 |
| Etanol | Powszechny alkohol używany jako paliwo i w perfumach. | 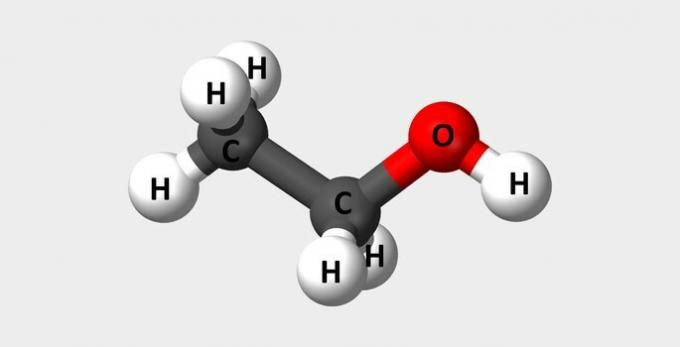 |
DO2H6O |
Koniecznie sprawdź te teksty na tematy związane z tym, czego się właśnie nauczyłeś:
- Biomolekuły
- Związki organiczne
- Masa cząsteczkowa
- Reguła oktetu
- Wiązania chemiczne
- Polaryzacja połączenia
- Siły międzycząsteczkowe