Istnieje kilka sposobów na przedstawienie tego samego związku chemicznego, odbywa się to za pomocą wzoru chemicznego, który może dostarczyć nam pewnych informacji o substancji, którą reprezentuje.
Poznamy teraz 5 form prezentacji związku na przykładzie substancji organicznej Benzen.
płaska formuła strukturalna: Jest to wzór opisujący wszystkie pierwiastki obecne w cząsteczce złożonej i ułożenie atomów poprzez płaskiej reprezentacji pary elektronów, które tworzą wiązanie chemiczne, są reprezentowane przez kreski. (─). Powyższy wzór strukturalny pokazuje, w jaki sposób atomy tworzące benzen są ze sobą połączone.

formuła molekularna: W formule tego typu element jest reprezentowany przez jego symbol, po którym następuje indeks (numer indeksu dolnego) wskazujący liczbę atomów obecnych w każdej cząsteczce. Mamy więc liczbę atomów tworzących substancję, jak widzimy, w cząsteczce benzenu znajduje się 6 węgli (C) i 6 wodoru (H).

wzór empiryczny: to jak „podsumowany” sposób przedstawiania związków. Prosta struktura pozwala jedynie zrozumieć kształt struktury benzenu i obecność nienasyceń (wiązań podwójnych).

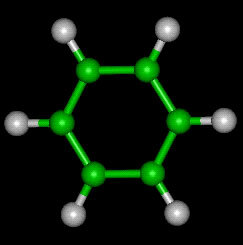
Formuła struktury kuli: w ten sposób węgle i wodory są identyfikowane przez kolor i rozmiar, gdzie C są reprezentowane przez kolor czarny, a H przez kolor biały.


Formuła w strukturze uderzenia i piłki ball
Ta ostatnia reprezentacja jest najczęściej używana do wstawiania przedmiotu chemii organicznej, na to pozwala obserwuj kształt struktury i nadal wizualizuj rodzaj wiązania, które łączy wodory z łańcuchem Główny.
W rzeczywistości są na rynku części do układania struktury linii i kulek, jakby to była układanka, gdzie nauczyciel może zademonstrować krok po kroku powstawanie związków organicznych.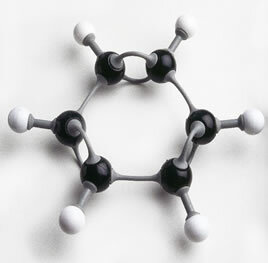
Zdjęcie pierścienia benzenowego zmontowanego z częściami z tworzywa sztucznego: doskonały materiał dydaktyczny do pracy w klasie.
Liria Alves
Absolwent chemii
Brazylijska drużyna szkolna
Zobacz więcej!
Wzory strukturalne węgla
wzory chemiczne
Chemia ogólna - Chemia - Brazylia Szkoła
Źródło: Brazylia Szkoła - https://brasilescola.uol.com.br/quimica/classificacao-das-formulas.htm
