Funkcje azotu to jedna z 4 grup funkcyjnych związków organicznych. Związki należące do tej funkcji są tworzone przez azot, dlatego nazywane są związkami azotowymi. Główne z nich to aminy, amidy, nitryle i związki nitrowe.
Aminy
W aminy to związki organiczne występujące w stanie stałym, ciekłym lub gazowym. Powstają w wyniku rozkładu zwierząt i można je również znaleźć w związkach ekstrahowanych z roślin.
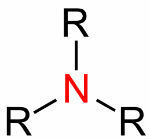
Ogólna formuła amin
Pochodzą od arylu lub alkilu w połączeniu z azotem. Aryl i alkil zastępują atomy wodoru. Zgodnie z tym zamiennikiem można je sklasyfikować w następujący sposób:
- Pierwotny: gdy zastąpiony jest tylko jeden wodór (R-NH2). Przykład: metanamina.
- Wtórny: gdy zastąpione zostaną dwa wodory (R1R2NH). Przykład: dimetanoamina.
- Trzeciorzędowy: gdy zastąpione są trzy wodory (R1R2R3N). Przykład: trimetanoamina.
Aminy są wykorzystywane do produkcji barwników, leków i mydeł.
Nomenklatura amin ma następującą postać:
- zastąpienie przyrostka węglowodorowego „o” słowem amina.
- wskazując pozycję azotu.
- wskazując rodzaj oprawy an, en lub in.
amidy
W amidy to związki organiczne, które można znaleźć w stanie stałym lub ciekłym. Pochodzą z acylu związanego z azotem i są produkowane w laboratorium.
Wzór cząsteczkowy amidów to CONH2, który jest reprezentowany w następujący sposób:
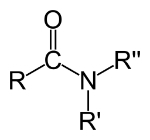
Ogólna formuła amidów
Amidy są klasyfikowane według liczby acylów związanych z azotem, które mają:
- Podstawowy: gdy ma tylko jedną grupę acylową R-CO)NH2.
- Wtórne: gdy mają dwie grupy acylowe (R-CO)2NH.
- Trzeciorzędowe: gdy mają trzy grupy acylowe (R-CO)3N.
Jeśli chodzi o liczbę obecnych grup amidowych, klasyfikacja jest następująca:
Diamidy, gdy występują dwie grupy amidów i triamidy, gdy występują trzy grupy amidów itp.
Jego zastosowania w życiu codziennym: m.in. produkcja kosmetyków pielęgnacyjnych (żel pod prysznic) i środków czyszczących (detergentów).
Nazwę amidów tworzy przedrostek, który wskazuje liczbę węgli. Następnie przyrostek „oico” dla węglowodoru zastępuje się słowem amid.
Związki nitro
Związki nitro to związki organiczne występujące w stanie ciekłym, które nie rozpuszczają się w wodzie, ponieważ są gęste i bardzo reaktywne. Ogólny wzór na związki nitrowe to NA2.
Aplikacja związków nitro jest kompleksowa. Stosowane są jako materiał wybuchowy, jako rozpuszczalnik, a także do produkcji maści i narzędzi.
Nazwę związków nitro tworzy się przez połączenie nazwy głównego łańcucha ze słowem nitro.
Nitryle
Nitryle, zwane również cyjankami, to związki organiczne występujące w stanie stałym i rozpuszczalne w wodzie. Ogólny wzór nitryli to R — C ≡ N.
Związki te wykorzystywane są w produkcji gumy, barwników, nawozów i tworzyw sztucznych.
Nazwę nitryle tworzy się przez połączenie nazwy węglowodoru ze słowem nitryl.
Przeczytaj też Funkcje natlenione.
Ćwiczenia
1. (Cesgranrio-RJ) Na początku 1993 roku gazety donosiły, że kiedy ktoś się zakochuje, organizm syntetyzuje substancję - etylofenyloaminę, odpowiedzialną za charakterystyczne jej wzbudzenie stan.
Klasyfikacja i charakter chemiczny tej aminy to odpowiednio:
a) amina pierwszorzędowa – kwas.
b) amina pierwszorzędowa – zasadowa.
c) amina drugorzędowa – obojętna.
d) amina drugorzędowa – kwas.
e) amina drugorzędowa – zasadowa.
Alternatywa e: amina drugorzędowa – zasadowa.
2. (UnB-DF) Acetoaminofen jest substancją o właściwościach przeciwbólowych i przeciwgorączkowych. Jest sprzedawany pod nazwą Tylenol, a jego formułę przedstawiono poniżej:
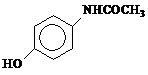
Zaznacz prawidłowe alternatywy dotyczące acetoaminofenu.
1. Należy do klasy fenoli;
2. Zawiera również funkcję amidową;
3. Ma wzór C8H9NA2;
4. Należy do klasy substancji aromatycznych ze względu na obecność pierścienia benzenowego.
Wszystkie alternatywy są poprawne


