Węgiel jest pierwiastkiem chemicznym o liczbie atomowej (Z) równej 6, co oznacza, że tworzące go atomy mają w swoim jądrze sześć protonów. Jego masa molowa wynosi 12,011 g/mol, a w naturze występują trzy izotopy węgla, którymi są: o węgiel-12, węgiel-13 i węgiel-14. C-12 ma sześć protonów i sześć neutronów w jądrze i jest najliczniejszy.
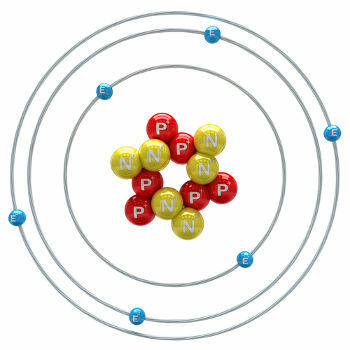
ilustracja atomu węgla 12
C-13 ma siedem neutronów i jest najmniej obfity (1,01 do 1,14%). C-14 ma osiem neutronów i jest pierwiastek radioaktywny emituje cząstki β (elektrony), powstające w stratosferze Ziemi, gdy neutrony promieniowania kosmicznego bombardują azot-14 obecny w tych górnych warstwach atmosfery. Jest on włączany przez wszystkie rośliny i zwierzęta, a wiedząc, że jego okres półtrwania wynosi około 5730 lat, jest używany do określenia wieku skamieniałości między 100 a 40 000 lat. Więcej szczegółów na temat C-14 i techniki datowania można zobaczyć w tekście. Co to jest węgiel-14?
Węgiel jest czterowartościowy, co oznacza, że potrzebuje czterech więcej protonów w swojej warstwie walencyjnej (warstwa najbardziej zewnętrzna), aby przestrzegać zasady oktetu. Dlatego zwykle tworzy cztery wiązania kowalencyjne, dzieląc cztery pary elektronów z innymi pierwiastkami, a także innymi węglami. Wiązania te mogą być pojedyncze, podwójne lub potrójne i skutkować powstaniem milionów różnych związków. Z tego powodu powstał obszar Chemii,
Chemia organiczna, który bada główne związki pochodzące z węgla, z wyjątkiem niektórych przypadków pochodzenia mineralnego, takich jak dwutlenek węgla (CO2), O tlenek węgla (CO), O węglan wapnia (CaCO3), wodorowęglan sodu lub wodorowęglan sodu (NaHCO3), miedzy innymi. Związki te są badane w Chemia nieorganiczna.Węgiel wykonuje alotropię, tworząc proste substancje, czyli substancje, które powstają tylko przez wiązania między atomami węgla. Istnieje co najmniej siedem alotropów węgla, którymi są grafit (alfa i beta), diament, lonsdaleit (diament heksagonalny), chaoit, węgiel (VI) i fulereny. W rzeczywistości istnieje kilka rodzajów fulerenów, które są syntetycznymi alotropowymi formami węgla. Mają strukturę wielościenną z atomem węgla na każdym wierzchołku, a przykładem jest DO60 nazywa buckminsterfullerene, a jego struktura przypomina piłkę nożną.
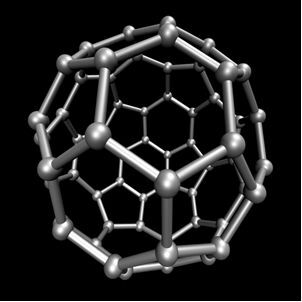
Carbon-60 (bukminsterfulleren)
Jednak wśród tych alotropów węgla są tylko dwa, które są naturalne. grafitJest od Diament. Różnią się jedynie krystalicznym ułożeniem atomów w przestrzeni, jak pokazano na poniższym rysunku, a to skutkuje zupełnie innymi właściwościami fizykochemicznymi. Przeczytaj tekst alotropia węgla po więcej informacji.

Dwie naturalne alotropowe formy węgla to grafit i diament.
Inną syntetyczną alotropową formą węgla jest nanorurki (zdjęcie poniżej), które mają szerokie zastosowania biologiczne, w tym diagnostykę medyczną i leczenie.

Ilustracja mikroskopijnej nanorurki węglowej
A zatem, węgiel jest obecny we wszystkim wokół nas i w nas, bo on komponuje naturalne związki organiczne — takie jak paliwa kopalne, które obejmują ropa naftowa, węgiel i gaz ziemny oraz inne paliwa, takie jak etanol i biopaliwa – między innymi produkty rolne. kształt też syntetyczne związki organiczne, takich jak włókna syntetyczne, z których składają się tkaniny, leki, polimery z tworzyw sztucznych i gumy, środki owadobójcze, barwniki i wiele innych. W nas, zwierzętach i warzywach, węgiel tworzy bardzo ważne związki, takie jak węglowodany, takie jak cukier, glukoza i celuloza; białka, które tworzą np. DNA, a wraz z lipidami tworzą błony czerwonych krwinek i białych krwinek.
Wszystko to pokazuje znaczenie węgla dla podtrzymania życia. Ale wiąże się to również z negatywnymi aspektami, takimi jak nasilenie efekt cieplarniany i w konsekwencji globalne ocieplenie, to dlatego, że głównym złoczyńcą tych problemów jest jego związek dwutlenku węgla (CO2). Głównie ze względu na duże spalanie paliw kopalnych, które uwalniają ten gaz, stężenie CO2 w atmosferze wzrosła. Jako gaz cieplarniany powoduje wyżej wymienione problemy. Z drugiej strony dwutlenek węgla jest również obecny w reakcjach życiowych, takich jak fotosynteza i oddychanie.
Jennifer Fogaça
Absolwent chemii
Źródło: Brazylia Szkoła - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-carbono.htm
