W reakcje spalania są obecne w wielu aspektach naszego codziennego życia. Na przykład główne źródła wytwarzania energii wynikają ze spalania lub spalania niektórych paliw, takich jak m.in. etanol, benzyna, węgiel drzewny. Co więcej, energia, której potrzebujemy do przetrwania i wykonywania pracy, jest wynikiem reakcji spalania, które zachodzą w naszych komórkach, kiedy „spalamy” spożywane przez nas jedzenie.
Ale co jest potrzebne do reakcji spalania?
Potrzebne są trzy rzeczy:
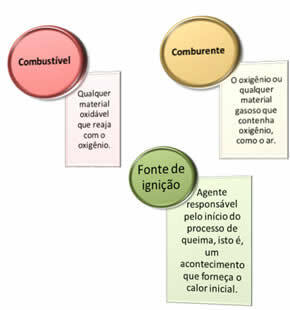
Te trzy czynniki składają się na trójkąt ognia, ponieważ po rozpoczęciu reakcji spalania uwolniona energia podtrzymuje reakcję i pozwala na jej kontynuowanie, aż paliwo, utleniacz lub ciepło (uwolniona energia) zniknie. Oznacza to, że będzie Reakcja łańcuchowa.
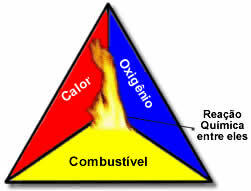
Na przykład, jeśli ktoś rzuci zapalonym papierosem do lasu, wybuchnie pożar (reakcja spalania). W tym przypadku Krzak to jest paliwo, O tlen obecny w powietrzu atmosferyczne jest utleniacz to jest papieros zapalił się źródło zapłonu. To spalanie będzie trwało, dopóki jeden z trzech czynników nie zostanie wyeliminowany. Jeśli strażacy rzucą wodę, upał zostanie wyeliminowany. Ale nawet jeśli nic nie zostanie zrobione, aby zatrzymać to spalanie, skończy się ono w pewnym momencie, czyli gdy skończy się paliwo (las).
Jak już wspomniano, w reakcjach tych uwalniane jest ciepło, dlatego spalanie jest reakcją egzotermiczną. Jednak ten rodzaj reakcji to niecałkowite spalanie. Aby zrozumieć dlaczego, zobacz różnicę między całkowitym a niepełnym spalaniem:
Teraz nie przestawaj... Po reklamie jest więcej ;)
Całkowite spalanie:
Analizując związki organiczne jako paliwa, musimy:
| TEN całkowite spalanie nastąpi to, gdy łańcuch węglowy zostanie przerwany i wszystkie atomy węgla w łańcuchu węglowym zostaną całkowicie utlenione. |
| ty produkty formowane przez węglowodory będą WSPÓŁ2 (dwutlenek węgla) i H2O (Woda). |
Obserwuj całkowite spalanie izooktanu, który jest jednym ze składników benzyny.
DO8H18(g) +25/2 O2 (g) → 8 CO2(g) + 9 rano2O(1)
Niepełne spalanie
| W tym przypadku nie ma wystarczającej ilości utleniacza, czyli wystarczającej ilości tlenu, aby spalić całe paliwo. |
| Tak więc powstałe produkty są WSPÓŁ (tlenek węgla) i H2O. |
Zaobserwuj jednak samo spalanie izooktanu, teraz nie do końca:
DO8H18(g) + 17/2 O2(sol) → 8 CO (sol) + 9 rano2O(1)
Przykładem jest wypalanie lasów, ponieważ powstające emisje składają się z CO i określonej materii, takiej jak sadza (C), a także popiołu i innych prostych i złożonych związków organicznych. Tlenek azotu, ozon i aldehydy mogą również powstawać w wyniku reakcji wtórnych z powodu obecności innych składników w powietrzu.
DO8H18(g) + 9/2 O2 (g) → 8C (sol) + 9 rano2O(1)
Jennifer Fogaça
Absolwent chemii
Brazylijska drużyna szkolna
Czy chciałbyś odnieść się do tego tekstu w pracy szkolnej lub naukowej? Popatrz:
FOGAÇA, Jennifer Rocha Vargas. „Całkowite i niepełne spalanie”; Brazylia Szkoła. Dostępne w: https://brasilescola.uol.com.br/quimica/combustao-completa-incompleta.htm. Dostęp 27 czerwca 2021 r.



