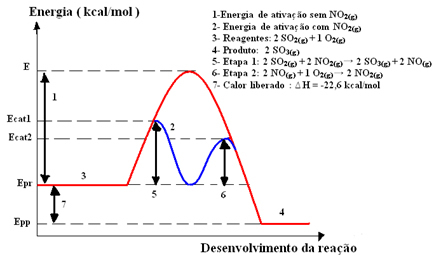
Katalizatory to substancje zdolne do przyspieszania reakcji bez zmiany, to znaczy nie są zużywane podczas reakcji.
Aby zrozumieć, jak działają katalizatory, musimy pamiętać o tym, co zostało wyjaśnione w tekście”Energia aktywacji”. Jak tam pokazano, aby reakcja chemiczna mogła się rozpocząć, konieczne jest, aby reagenty miały lub otrzymały określoną ilość energii minimalnej, która nazywa się energia aktywacji.
Przy tej minimalnej energii reagenty są w stanie osiągnąć kompleks aktywowany, który jest stanem pośrednim (stanem przejściowym), który powstaje między substratami i produktami, w którym struktury istnieją osłabione dotychczasowe powiązania i tworzenie nowych powiązań (obecne w produkty).
Rozważmy na przykład poniższą ogólną reakcję:
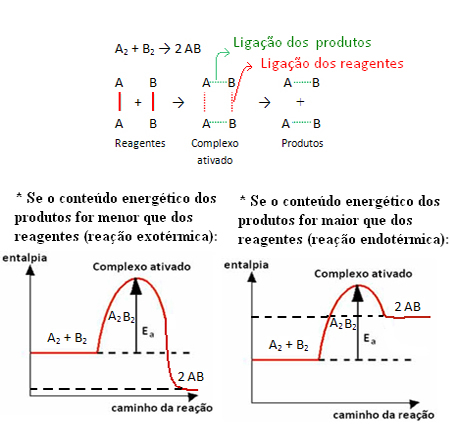
Należy zauważyć, że energia aktywacji potrzebna do dotarcia do aktywowanego kompleksu staje się rodzajem przeszkody, którą należy pokonać, aby zaszła reakcja. Oznacza to, że im większa energia aktywacji reakcji, tym większa przeszkoda do pokonania i wolniejsza szybkość reakcji.
Jest też odwrotnie, im energia aktywacji jest mniejsza, reakcja będzie szybsza. Dokładnie to katalizatory czy oni tworzą alternatywną ścieżkę, która wymaga mniejszej energii aktywacji, dzięki czemu reakcja przebiega szybciej.
Teraz nie przestawaj... Po reklamie jest więcej ;)

W celu obniżenia energii aktywacji katalizator działa poprzez zmianę mechanizmu reakcji, łącząc z odczynnikami w układzie, który może być jednofazowy (kataliza jednorodna) lub wielofazowy (kataliza heterogeniczna).
Więcej szczegółów na temat tego typu katalizy można zobaczyć w poniższych tekstach:
- kataliza jednorodna
- kataliza heterogeniczna
Ale ogólnie można powiedzieć, że to that Połączenie reagenta i katalizatora tworzy związek pośredni, który następnie przekształca się, dając początek produktowi i katalizatorowi. Zwróć uwagę, jak można to przedstawić:
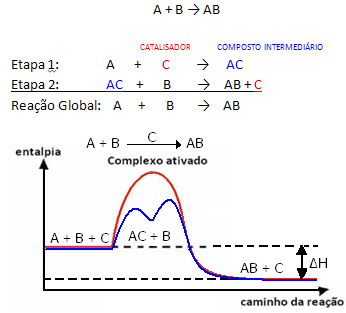
Zobacz, że katalizator jest regenerowany pod koniec reakcji, a nie jest przez niego zużywany.
Ważnym faktem jest to, że katalizator przyspiesza zarówno reakcje do przodu, jak i do tyłu, co oznacza, że zmniejsza energię aktywacji obu.
Jennifer Fogaça
Absolwent chemii
Czy chciałbyś odnieść się do tego tekstu w pracy szkolnej lub naukowej? Popatrz:
FOGAÇA, Jennifer Rocha Vargas. „Jak działają substancje katalityczne?”; Brazylia Szkoła. Dostępne w: https://brasilescola.uol.com.br/quimica/como-atuam-as-substancias-catalisadoras.htm. Dostęp 27 czerwca 2021 r.