Nazwa chemiczna Witamina C é kwas L-askorbinowy, lub po prostu Kwas askorbinowy. Ta nazwa przekazuje chemiczne i biologiczne role tego związku. Aspekt chemiczny polega na tym, że jest kwaśny, ponieważ zawiera w swojej strukturze grupę fenolowo-hydroksylową. Grupa fenolowa przyłączona do trzeciego węgla w łańcuchu ulega jonizacji w roztworze wodnym, jak pokazano poniżej, uwalniając jon hydroksonu (H3O+), co jest charakterystyczne dla zachowania kwasowego:
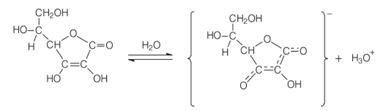
Słowo „askorbinowy” pochodzi od jego biologicznej właściwości do zwalczania choroby zwanej szkorbutem. A „L” pochodzi z faktu, że kwas askorbinowy ma asymetryczne centrum przy węglu 5, wykazując aktywność optyczną. Jednak jego działanie przeciw szkorbutowi wywodzi się prawie całkowicie z izomeru L (lewogyro), który ma w wodzie rotację właściwą 24°.
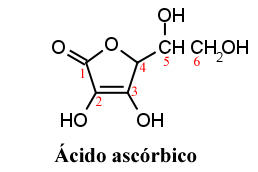
Kwas askorbinowy został po raz pierwszy wyizolowany przez węgierskiego badacza Szent-Györgi w 1922 roku jako biały krystaliczny proszek.
Ludzie i inne zwierzęta, takie jak małpy, niektóre ptaki i niektóre ryby, nie mogą syntetyzować witaminy C. Niedobór tej witaminy w organizmie prowadzi do wadliwej syntezy tkanki kolagenowej i wspomnianej choroby,
szkorbut.Pomiędzy główne źródła witaminy C, mamy świeże owoce, takie jak m.in. wiśnia, nerkowiec, guawa, czarna porzeczka, mango, pomarańcza, acerola, pomidor. Ziemniaki są również doskonałym źródłem witaminy C, podobnie jak papryka i warzywa liściaste (bertalha, brokuły, jarmuż, rzepa, liście manioku i pochrzyn).

Mówimy „owoce świeży”, ponieważ witamina C może zostać częściowo lub całkowicie zniszczona podczas długich okresów przechowywania. Na przykład co miesiąc przechowywany ziemniak traci 15% swojej witaminy C. Ponadto ciepło może go również zniszczyć. Żywność długo gotowana i żywność, która została przetworzona przemysłowo, zawiera mało witaminy C. W przypadku ziemniaków, jeśli są gotowane bez skórki, natychmiast tracą od 30% do 50% swoich właściwości.
Jedną z głównych właściwości kwasu askorbinowego jest jego zdolność do działania jako środek redukujący. Ponieważ ma wyjątkową łatwość utleniania w roztworze wodnym, jest silnym środkiem przeciwutleniacz, ponieważ może utleniać się w miejsce innych związków.
Na przykład w życiu codziennym, gdy kroimy niektóre owoce, takie jak gruszki, banany i jabłka, z czasem ciemnieją. Dzieje się tak, ponieważ owoce te zawierają enzym oksydazę polifenolową, który powoduje enzymatyczne utlenianie naturalnych związków fenolowych w obecności tlenu cząsteczkowego, tworząc chinon. Polimeryzują i wytwarzają melaniny, które są dokładnie ciemnymi, nierozpuszczalnymi pigmentami, które widzimy w tych owocach.
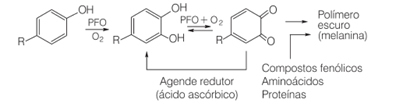
Jednym ze sposobów hamowania działania enzymu oksydazy polifenolowej jest dodatek kwasu askorbinowego. Dzieje się tak np. gdy do sałatki owocowej dodamy sok pomarańczowy.
W obecności tlenu i katalizatora kwas askorbinowy utlenia się, stając się kwas dehydroaskorbinowy. Kwas ten ma pH poniżej 4, a obniżenie pH tkanki owocowej powoduje spowolnienie reakcji brązowienia. Przy pH poniżej 3 nie ma aktywności enzymatycznej.
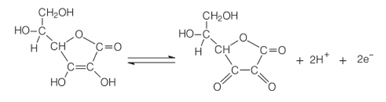
Ta właściwość witaminy C jest szeroko stosowana w przemysł spożywczy aby zapobiec pojawieniu się nieprzyjemnego smaku, toksyczności oraz ze względów ekonomicznych, ponieważ szacuje, że około 50% utraty owoców tropikalnych na świecie jest spowodowane enzymem polifenolowym oksydaza.
Ze względu na rolę antyoksydacyjną witaminę C stosuje się również w kosmetyki. Jego miejscowe stosowanie poprzez te kosmetyki pozwala osiągnąć poziom, który nie jest możliwy przy doustnym przyjmowaniu samej witaminy C. Chroni skórę przed promieniami UV i wolnymi rodnikami, które prowadzą do przedwczesnego starzenia.

Jennifer Fogaça
Absolwent chemii
Źródło: Brazylia Szkoła - https://brasilescola.uol.com.br/quimica/composicao-aplicacoes-vitamina-c.htm

