Ciepło właściwe to wielkość badana przez fizykę, która wiąże ilość ciepła odbieranego przez substancję i jej zmienność termiczną.
Nazywany również pojemność cieplna, ta wielkość wskazuje ilość ciepła potrzebną, aby gram dowolnej substancji uległ zmianie temperatura odpowiadająca 1°C, oprócz wskazania zachowania materiału pod wpływem źródła ciepła.
Ciepło właściwe jest bezpośrednio związane z obszarem fizyki zwanym Kalorymetria, który bada transfery energii z ciała o wyższej temperaturze do innego ciała o niższej temperaturze.
W niniejszym opracowaniu ciepło właściwe występuje w definicji ciepła jawnego i pojemności cieplnej materiał, ponieważ niektóre zjawiska można lepiej zrozumieć z definicji ciepła konkretny.
A im większe ciepło właściwe, tym większa ilość ciepła, które trzeba dostarczyć lub usunąć z substancji, aby miała ona zmienność termiczną.
Na przykład woda w porównaniu z innymi substancjami ma najwyższe ciepło właściwe, odpowiadające 1 cal/g.ºC.
Tabela porównawcza poszczególnych wartości cieplnych
Inne substancje i materiały również mają swoje własne wartości cieplne, jak pokazano w poniższej tabeli:
| Substancja | Ciepło właściwe (cal/g.ºC) |
| woda | 1 cal/g.°C |
| Alkohol etylowy | 0,58 cal/g.°C |
| Aluminium | 0,22 cal/g.°C |
| Powietrze | 0,24 cal/g.°C |
| Piasek | 0,2 kcal/g.°C |
| Węgiel | 0,12 cal/g.°C |
| Prowadzić | 0,03 cal/g.°C |
| Miedź | 0,09 cal/g.°C |
| Żelazo | 0,11 cal/g.°C |
| lód | 0,50 cal/g.°C |
| Wodór | 3,4 cal/g.°C |
| drewno | 0,42 cal/g.°C |
| Azot | 0,25 cal/g.°C |
| Tlen | 0,22 cal/g.°C |
| Szkło | 0,16 cal/g.°C |
Specyficzna formuła ciepła
Aby poznać ciepło właściwe substancji, konieczne jest zastosowanie następującego wzoru:
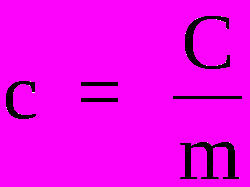
Gdzie,
do - ciepło właściwe (cal/g°C lub J/Kg.K)
DO - pojemność cieplna (cal/°C lub J/K)
mi - masa (g lub kg)
W systemie międzynarodowym (SI) ciepło właściwe jest mierzone w J/kg. K (dżul na kilogram i na kelwin). Jednak najczęściej używaną miarą jest cal/g°C (kalorie na gram i na stopień Celsjusza).
Zobacz także znaczenie ciepło i temperatura.
