Kiedy mówimy o pH, odnosimy się do potencjału hydrogenionowego roztworu, czyli ilości kationów hydroniowych (H+ lub H3O+), które są zdyspergowane w rozpuszczalniku roztworu.
Kationy hydroniowe są dobrze znane z definicji zaproponowanej przez naukowca Arhenius na kwas. Ten naukowiec twierdzi, że kwas czy każda substancja jest w stanie? zjonizować i wytwarzają jony hydroniowe w środowisku wodnym.
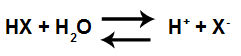
Równanie jonizacji kwasu
akronim pH służy jako odniesienie do określenia poziomu kwasowości pożywki. Ale od dawna chemicy również stosowali pH jako odniesienie do określenia, oprócz kwasowości, czy podłoże jest zasadowe czy obojętne.
Jest to możliwe, ponieważ chemicy są teraz świadomi, że woda ulega samojonizacji, czyli wytwarza hydronie (H+) i wodorotlenki (OH-). Tak więc roztwór wodny nigdy nie zawiera tylko hydronu lub wodorotlenku, ale jedno i drugie, co widać z następującego równania:

Równanie autojonizacji wody
Wartości używane jako odniesienie dla pH
Wartości używane dla pH odnoszą się do stałej jonizacji (Kw) wody o temperaturze 25
OC, co jest równe 10-14. W tej temperaturze stężenia jonów hydroniowych i wodorotlenowych wytwarzanych przez wodę są absolutnie równe, czyli 10-7 mol/L.[H+]=[OH-]= 10-7
Z tego odniesienia, wartości stosowane dla zakresu pH od 0 do 14.
Wzory do obliczania pH
a) Obliczenie ze stężenia w mol/L kationów hydroniowych
Obliczenie wartości pH można wykonać bezpośrednio, o ile znamy stężenie hydroniów ([H+]). Popatrz:
pH = -log[H+]
lub
10-pH = [H+]
b) Obliczanie ze stężenia anionów wodorotlenowych (OH-)
pOH = -log[OH-]
lub
10-pOH = [OH-]
Po obliczeniu wartości pOH należy użyć jej w poniższym wyrażeniu, aby określić wartość pH.
pH + pOH = 14
Interpretacja wartości pH
Znając wartość pH możemy określić, czy dany roztwór ma charakter kwasowy, zasadowy czy obojętny. W tym celu użyj następującej schematycznej zależności:
Dla wartości pH poniżej 7 = środowisko kwaśne;
Dla pH o wartości równej 7 = medium neutralne;
Dla wartości pH powyżej 7 = pożywka podstawowa.
Przykłady
Pierwszy przykład: Wiedząc, że stężenie kationów hydroniowych w roztworze wynosi 2,10-4 mol/L, jaka powinna być wartość pH tego roztworu?
Aby określić wartość pH roztworu na podstawie stężenia hydroniów (H+), 2.10-4 mol/L, musimy użyć następującego wyrażenia:
pH = -log[H+]
pH = -log[2,10-4 ]
pH = –(log 2 + log 10-4)
pH = -log2 - log10-4
pH = –log 2 – 4,log 10
pH = –0,3 + 4.(1)
pH = -0,3 + 4
pH = 3,7
Drugi przykład: Roztwór utworzony przez pewną substancję rozpuszczoną ma stężenie jonów wodorotlenowych równe 10-11 mol/L. Z tego stężenia możemy powiedzieć, że pH tego roztworu jest warte ile?
Aby określić wartość pH roztworu ze stężenia wodorotlenku, 10-11 mol/L, musimy wykonać następujące czynności:
1O Krok: obliczyć wartość pOH.
10-pOH = [OH-]
10-pOH = 10-11
Musimy pomnożyć wyrażenie przez -1, ponieważ pOH jest zawsze dodatnią niewiadomą.
-pOH = -11.(-1)
pOH = 11
2O Krok: obliczyć wartość pH.
pH + pOH = 14
pH + 11 = 14
pH = 14 - 11
pH = 3
Przeze mnie Diogo Lopes Dias
Źródło: Brazylia Szkoła - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-ph.htm