O kwas mrówkowy otrzymuje swoją nazwę, ponieważ po raz pierwszy uzyskano ją przez destylację czerwonych mrówek (z łac. formica = mrówka), które wstrzykują kwas karboksylowy przez ugryzienie, powodując silny ból, obrzęk i swędzenie.
Jednak jego oficjalna nomenklatura to kwas metanowy, którego wzór strukturalny przedstawiono poniżej:

Oprócz mrówek kwas metanowy znajduje się również w pszczołach, pokrzywach, sosnach i niektórych owocach.
W temperaturze pokojowej jest bezbarwny, płynny, żrący, silnie pachnący i drażniący. Kwas ten stosowany jest jako zaprawa, przy produkcji tlenku węgla, w leczeniu reumatyzmu, w produkcji kwasu szczawiowego, jako środek bakteriobójczy, jako środek dezynfekujący oraz w produkcji innych produktów Organiczny.
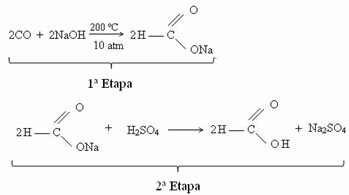
Obecnie kwas mrówkowy otrzymuje się w reakcji tlenku węgla z sodą kaustyczną. Ta reakcja jest techniką podobną do tej opracowanej w 1855 roku przez francuskiego chemika Marcellina Berthelota (1827-1907). Dalej mamy tę reakcję, w której najpierw otrzymuje się metanolan sodu, który po reakcji z kwasem siarkowym, jako jeden z produktów wytwarza kwas metanowy:
Teraz nie przestawaj... Po reklamie jest więcej ;)
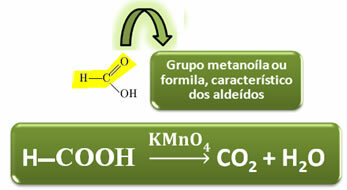
W przeciwieństwie do innych kwasów karboksylowych, kwas mrówkowy posiada grupę funkcyjną aldehydów, co nadaje mu właściwość działania jako reduktor. Redukuje reakcje Fehlinga i Tollensa, utleniając się do dwutlenku węgla i wody.
Jennifer Fogaça
Absolwent chemii
Czy chciałbyś odnieść się do tego tekstu w pracy szkolnej lub naukowej? Popatrz:
FOGAÇA, Jennifer Rocha Vargas. "Kwas mrówkowy"; Brazylia Szkoła. Dostępne w: https://brasilescola.uol.com.br/quimica/Acido-formico.htm. Dostęp 28 czerwca 2021 r.



