TEN geometria molekularna, czyli ułożenie atomów w cząsteczce można określić za pomocą reguły chemika Gillespie, w którym wymienia liczbę atomów przyłączonych do centralnego atomu i liczbę chmur elektronika.
Wiedza o geometrii cząsteczki jest niezwykle ważna, ponieważ pomaga nam określić biegunowość, a co za tym idzie rozpuszczalność (zgodnie z zasadą podobnych rozpuszcza się) podobny).
z wezwaniem geometria czworościenna, nie jest inaczej. Zobacz kryteria określania go zgodnie z zasadami Gillespiego:
Cząsteczki pięcioatomowe (pięć atomów);
Brak chmur elektronowych w centralnym atomie;
cząsteczki złożone lub złożone aniony.
Trochę przykłady cząsteczek o geometrii czworościennej oni są:
CH4

Wzór strukturalny CH4
Węgiel ma cztery elektrony w swojej powłoce walencyjnej i wszystkie te elektrony wiążą się z wodorami. Dlatego węgiel nie ma chmury elektronicznej (dodatkowa para elektronów).
TYLKO4-2
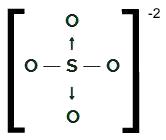
Wzór strukturalny OS4-2
Siarka, która ma sześć elektronów w powłoce walencyjnej, tworzy dwa pojedyncze wiązania z dwoma atomami tlenu i dwoma
datywne wiązania kowalencyjne z pozostałymi dwoma tlenami. W wiązaniach pojedynczych używa dwóch swoich elektronów, aw każdym celowniku wykorzystuje kolejne dwa (łącznie cztery elektrony zaangażowane w celowniki), w sumie sześć elektronów. W związku z tym nie ma już żadnej chmury.NH4+

Wzór strukturalny NH4+
Azot, który ma pięć elektronów w powłoce walencyjnej, tworzy trzy pojedyncze wiązania z atomami wodoru i wiązanie celowane z drugim wodorem. W wiązaniach pojedynczych wykorzystuje trzy ze swoich elektronów, a w celowniku wykorzystuje kolejne dwa, w sumie pięć elektronów. W związku z tym nie ma już żadnej chmury.
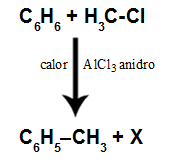
CH3Cl
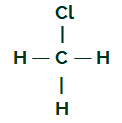
Wzór strukturalny CH3Cl
Teraz nie przestawaj... Po reklamie jest więcej ;)
Węgiel ma cztery elektrony w powłoce walencyjnej i wszystkie te elektrony wiążą się z wodorami i atomem chloru. Z tego powodu węgiel nie ma chmury elektronicznej.
→ Polaryzacja cząsteczki
Wiedząc, że dana cząsteczka ma geometrię czworościenną, możemy określić jej biegunowość niezwykle prosta forma, ponieważ cząsteczka ma zajęte cztery bieguny (cztery ligandy w atomie) centralny). W tym celu wystarczy znać charakterystykę segregatorów i wziąć pod uwagę jedną z następujących zasad:
Jeśli liczba chmur jest równa liczbie równych ligandów = cząsteczka niepolarna;
Jeśli liczba chmur różni się od liczby równych ligandów = cząsteczka polarna.
W następujących dwóch cząsteczkach, których geometria jest czworościenna, możemy zastosować powyższe zasady i wskazać ich polaryzację:
Cząsteczka metanu
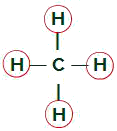
Równe ligandy w cząsteczce metanu
Cząsteczka metanu ma cztery chmury elektronowe (cztery pojedyncze wiązania), a także cztery atomy wodoru przyłączone do centralnego atomu. A zatem, mamyczterychmury i cztery równe spoiwa, wkrótce, cząsteczka jest niepolarna.
Obserwacja: Jeśli cząsteczka substancji jest apolat, dobrze rozpuszcza się w inną substancję, której cząsteczki również są niepolarny.
Cząsteczka chlorometanu

Równe ligandy w cząsteczce chlorometanu
Cząsteczka chlorometanu ma cztery chmury elektronów (cztery pojedyncze wiązania) i trzy atomy wodoru i jeden atom chloru przyłączony do centralnego atomu. A zatem, mamyczterychmury i trzy równe ligandy (trzy wodory); wkrótce cząsteczka jest polarna.
Obserwacja: Jeśli cząsteczka substancji jest polarny, dobrze rozpuszcza się w inną substancję, której cząsteczki również są polarny.
Przeze mnie Diogo Lopes Dias
Czy chciałbyś odnieść się do tego tekstu w pracy szkolnej lub naukowej? Popatrz:
DNI, Diogo Lopes. „Geometria czworościenna”; Brazylia Szkoła. Dostępne w: https://brasilescola.uol.com.br/quimica/geometria-tetraedrica.htm. Dostęp 28 czerwca 2021 r.