På amider er organiske forbindelser preget av tilstedeværelse av en nitrogen (N) direkte festet til en karbonyl (C = O). Dette er stoffer som er tilgjengelige på en naturlig måte, en av dem er i utskillelsen fra pattedyr (urea), men de kan også oppnås ved kunstig syntese.
Amider kan produseres, for eksempel ved ammoniumsalt dehydrering, prosess som brukes til fremstilling av polymerer. De brukes også som gjødsel, på grunn av tilgjengeligheten av nitrogener, og hvordan medikament, med antimikrobiell virkning.
Les mer:Akrylamid - amid som kan stamme fra oppvarming av noen matvarer
Amid struktur
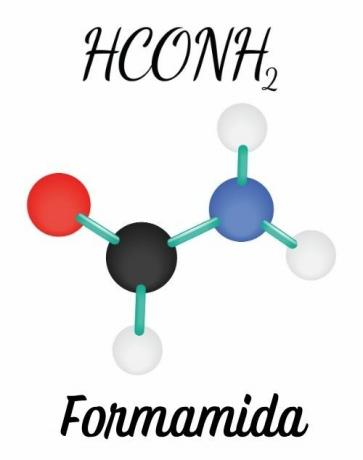
Amidene er dannet av en nitrogen bundet direkte til en karbonyl- eller acylgruppe (R-C = O). Dobbeltbåndet mellom karbon det er oksygen og muligheten for å flytte dette paret til nitrogen gir molekylet plan geometri, i motsetning til aminer, som har pyramidegetri.
Klassifisering av amider
Klassifisering i henhold til antall organiske substituenter
Samt aminer, amider er klassifisert i henhold til antall substituerende organiske radikaler som nitrogen harfor amider må vi imidlertid vurdere at en av gruppens ligander vil være acylgruppen, det vil si at vi bare vil ha amider av typen:
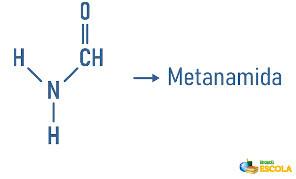
- Usubstituert amid: har nitrogen bundet til to hydrogener og en karbonylgruppe.
Eksempel:

- Monosubstituert amin: har nitrogen bundet til et hydrogen, en karbonylgruppe og en organisk radikal. I dette tilfellet, hvor ett av hydrogenene er erstattet av en karbonkjede, kan du vurdere R som en organisk gruppe.
Eksempel:

- Disubstituert amin: har nitrogen bundet til to organiske radikaler og en karbonyl. I dette tilfellet ble de to hydrogenene erstattet av karbonkjeder.
Eksempel:

Se også: Hvordan klassifisere organiske halogenider?
Klassifisering i henhold til antall karbonyler knyttet til nitrogen
Amider kan også klassifiseres etter antall karbonyler festet direkte til nitrogenet i molekylet.
- Primære amider: bare en acylgruppe koblet til nitrogen (R-CO) NH2 .
- sekundære amider: to karbonyler eller acylgrupper knyttet til nitrogen (R-CO)2NH.
- tertiære amider: tre acylgrupper knyttet til nitrogen (R-CO)3Nei.

Nomenklatur for amider
DE nomenklatur for amider vil bli gitt av:
prefiks som angir antall karbonatomer i kjeden + plassering og infiks som indikerer umettede (hvis noen) + amidavslutning |
Se tabellen nedenfor:
Prefiks (antall karbonatomer) |
Infix (kjedemetning) |
Suffiks (funksjonell gruppe) |
|||
1 karbon |
Møtte- |
Bare enkeltanrop |
-an- |
amider |
-amid |
2 karbonatomer |
Et- |
||||
3 karbonatomer |
Rekvisitt- |
1 dobbeltbinding |
-en- |
||
4 karbonatomer |
Men- |
||||
5 karbonatomer |
pent- |
2 dobbeltbindinger |
-dien- |
||
6 karbonatomer |
Hex- |
||||
7 karbonatomer |
Hept- |
1 trippelbinding |
-i- |
||
8 karbonatomer |
Okt- |
||||
9 karbonatomer |
Ikke- |
2 trippel lenker |
-diin- |
||
10 karbonatomer |
Des- |
Kulltallet må starte med siden nærmest nitrogenet i den funksjonelle gruppen.
Eksempler:



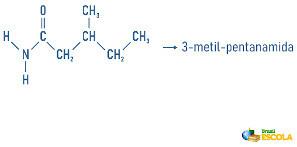
Aminer kan også motta en spesifikasjon på klassifiseringen av molekylet i nomenklaturen:
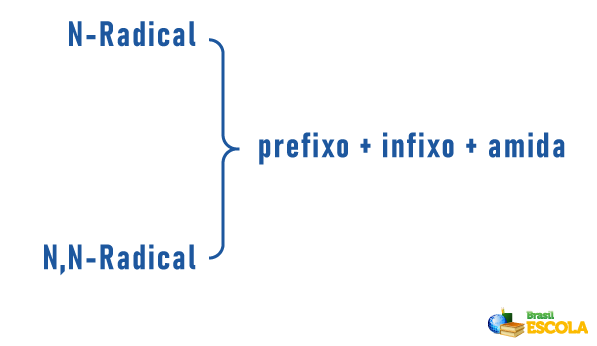
Husk at nomenklaturen for radikale er dannet av: Prefiks som angir antall karbon + avslutning “il” eller “ila”. Radikalene plasseres i nomenklaturen i alfabetisk rekkefølge.
Eksempler:


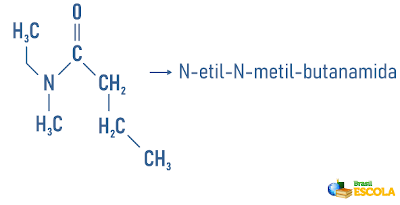
Også tilgang: Nomenklatur for sykliske og forgrenede hydrokarboner
Egenskaper av amider
- Høyt smelte- og kokepunkt, som vil ha en skalert verdi i henhold til størrelsen og det romlige arrangementet av karbonkjeden.
- Meget polær på grunn av tilstedeværelsen av karbonyl og nitrogen.
- Usubstituert og monosubstituert amid hydrogenbinding.
- Mindre og enklere molekyler er vannløselige. Molekylets størrelse forstyrrer også amidens løselighet: jo større karbonkjeden er, desto mindre oppløselig vil de være i vann.
- Amidene har en grunnleggende karakter på grunn av deres tilbøyelighet til å motta H-ioner+.
Påføring av amider
- Brukes som mellomledd i produksjonen av polyetylener som nylon.
- Brukes i formuleringen av medisiner som sulfanilamid og penicillin, aktive prinsipper for bakteriedrepende medisiner for infeksjonskontroll.
- Urea, som kan oppnås syntetisk eller som et produkt utskilt av pattedyr, er et stoff i amidgruppen, et diamid. Det brukes som kosttilskudd i landbruket og som gjødsel.

Å skaffe amidene
Amider finnes lett i en naturlig form, men deres syntetiske form er fortsatt mye brukt i industrielle prosesser. Nedenfor er noen amidproduksjonsreaksjoner basert på andre nitrogenholdige forbindelser.
Ammoniumsalt dehydrering reaksjon

Reaksjon av aminer med syreklorid
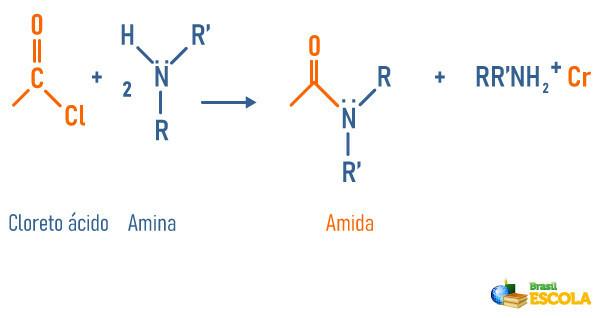
-
Reaksjon av anhydrider med aminer
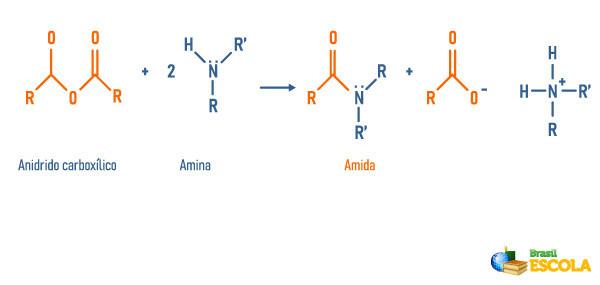
Reaksjon av estere med aminer

Strukturell omlegging av en aldoksim
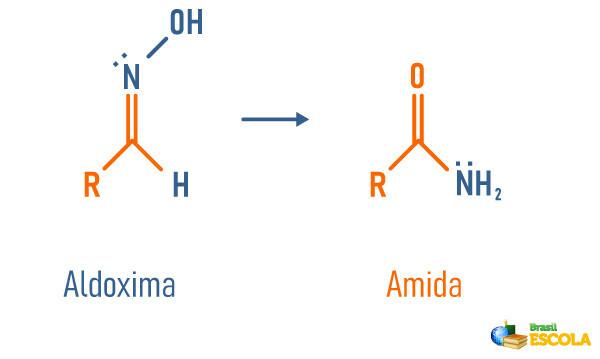
-
Nitrilhydrering
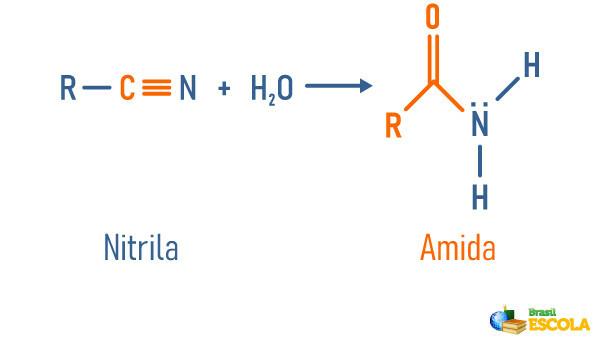
Les også: Amidhydrolyse - reaksjon som brukes til å oppnå viktige stoffer
løste øvelser
Spørsmål 1 - (UFRS) Aspartam, avbildet nedenfor, er et kunstig søtningsmiddel som brukes i mange brus og kalorifattig mat.

Gruppen innrammet i figuren er karakteristisk for den organiske funksjonen
A) ester.
B) amid.
C) aminosyre.
D) amin.
E) karbohydrat.
Vedtak
Alternativ B. Den funksjonelle gruppen valgt i figuren er et amid på grunn av tilstedeværelsen av karbonyl (C = O) koblet direkte til nitrogen (N).
Spørsmål 2 - (UNESP) I august 2005 ble det rapportert om beslag av batcher med lidokain som ville ha forårsaket flere menneskers død i Brasil på grunn av produksjonsproblemer. Dette legemidlet er et lokalbedøvelsesmiddel som er mye brukt i endoskopiske undersøkelser, og reduserer pasientens ubehag. Dens molekylære struktur er vist nedenfor:
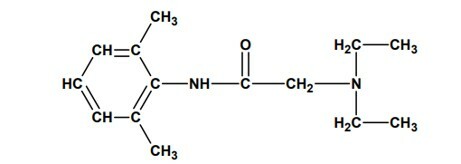
og presenterer funksjonene:
A) sekundær amin og tertiær amin.
B) amid og tertiær amin.
C) amid og ester.
D) ester og tertiær amin.
E) ester og sekundært amin.
Vedtak
Alternativ B.
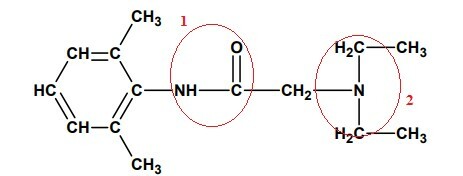
Etter å ha valgt og nummerert de karakteristiske delene av hver organiske funksjon, la oss analysere hver enkelt:
1 - Det er en AMIDA på grunn av tilstedeværelsen av acylgruppen, (R-C = O) direkte koblet til nitrogen, monosubstituert.
2- Da vi ikke har tilstedeværelse av acylgruppen (R-C = O), men bare nitrogenet bundet direkte til andre karbonatomer i denne gruppen vi har en tertiær amin, fordi alle tre hydrogenene, som tidligere var bundet til nitrogen, er erstattet av grupper Organisk.
Av Laysa Bernardes Marques de Araújo
Kjemilærer