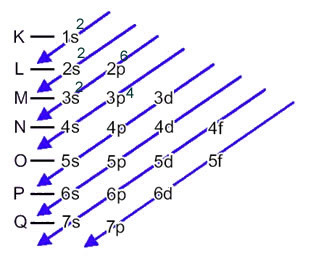
Den elektroniske fordelingen av et atoms elektroner i nøytral eller grunnleggende tilstand utføres ofte med Pauling-diagram, Vist under:
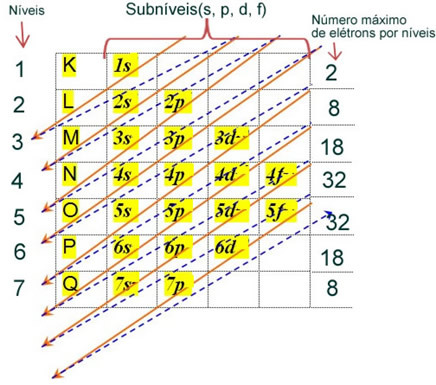
De detaljerte reglene for denne distribusjonen finner du i følgende to tekster på nettstedet vårt: “Elektronisk distribusjon av elektroner"og"Elektroniske distribusjonsregler”.
Den elektroniske distribusjonen av ioner fungerer i utgangspunktet på samme måte som for atomer i nøytral tilstand; med bare en forskjell. Siden et ion er et atom som har fått eller mistet elektroner, må vi ta hensyn til dette og gjøre følgende:

En viktig observasjon er: endringen er gjort på det ytterste undernivå og ikke den mest energiske.
hvis ionet er en kation, vi må fjern elektronene at han mistet. La oss se på et eksempel:
Jernatomet (atomnummer = 26) har følgende elektroniske fordeling i undernivåene i energisk rekkefølge: 1s2 2s2 2p6 3s2 3p6 4s2 3d6. Når det gjelder de elektroniske lagene, har vi: K =2; L = 8; M = 14; N = 2.
Denne fordelingen er vist i Pauling-diagrammet nedenfor:
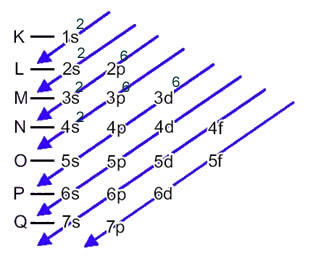
Når jernatomet mister 2 elektroner, blir det til Fe-kationen.2+. Så når du lager din elektroniske distribusjon, må vi fjern 2 elektroner fra det siste skallet(N) og ikke fra det mest energiske undernivået, som vist under:
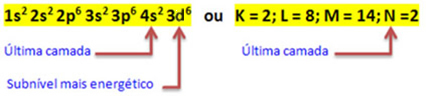
Dermed den elektroniske distribusjonen av Fe-kationen2+ er gitt av:
1s2 2s2 2p6 3s2 3p6 3d6 eller K = 2; L = 8; M = 14
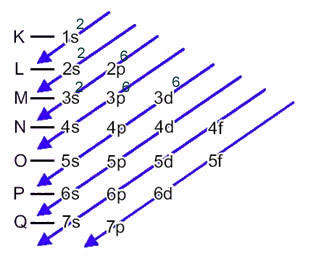
Nå, hvis vi må utføre den elektroniske distribusjonen av en anion, vi må legg til elektronene den mottok.Se hvordan dette gjøres i følgende eksempel:
Svovelanionet (16s2-) dannes fra svovelatomet (16S) ved forsterkning av 2 elektroner, som indikert ved ladning 2-. Dens elektroniske distribusjon på bakken er gitt av:
1s2 2s2 2p6 3s2 3p4 eller K = 2; L = 8; M = 6
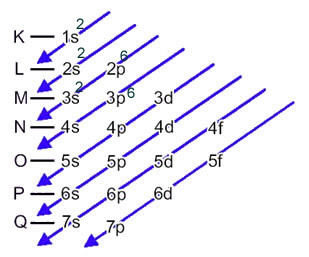
I dette tilfellet er det siste delnivået det samme som energidelenivået, 3p. Så vi legger til de to elektronene til svovelanionen:
1s2 2s2 2p6 3s2 3p6 eller K = 2; L = 8; M = 8
Av Jennifer Fogaça
Uteksamen i kjemi
Kilde: Brasilskolen - https://brasilescola.uol.com.br/quimica/distribuicao-eletronica-ions.htm
