dobbelt salt er navnet gitt til en av klassifiseringene som uorganiske salter kan motta. De andre klassifiseringene er: enkle, alun, hydroksylert, hydrogenert og hydrert. For å bli karakterisert som et dobbelt salt, må et uorganisk salt ha en av kombinasjonene beskrevet nedenfor:
En kation (Y) og to anioner (X og W), og er representert med følgende formel:
YXW
Et anion (X) og to kationer (Y og Z), og er representert med følgende formel:
YZX
Merk: Disse saltene dannes når en nøytraliseringsreaksjon utføres mellom to baser annerledes og en syre, eller mellom to forskjellige syrer og en base.
Navngivningsregel for dobbelt salt
Å nevne et dobbelt salt, det er først og fremst nødvendig å kjenne dens konstitusjon, fordi det for hver type dobbeltsalt er en spesifikk navneregel, som kan sees nedenfor:
a) Nomenklaturregel for dobbeltsalt med to kationer
Når en dobbelt salt har to kationer, må vi bruke følgende regel:

Nomenklaturregel brukt for dobbeltsalter med to kationer
Følgende er to eksempler på anvendelse av denne navngivningsregelen:
Første eksempel: Linje4s
Dette saltet består av:
Anion: sulfid (S-2);
Mer elektropositivt kation: litium (Li+1);
Mindre elektropositivt kation: ammonium (NH4+1).
Derfor er navnet litium (dobbelt) ammoniumsulfid.
Andre eksempel: RbCaBO3
Dette saltet består av:
Anion: borat (BO3-3);
Mer elektropositivt kation: rubidium (Rb+1);
Mindre elektropositivt kation: kalsium (Ca+2).
Dermed er navnet borat (dobbelt) av rubidium og kalsium.
b) Nomenklaturregel for dobbeltsalt med to anioner
Når en dobbelt salt har to anioner, må vi bruke følgende regel:
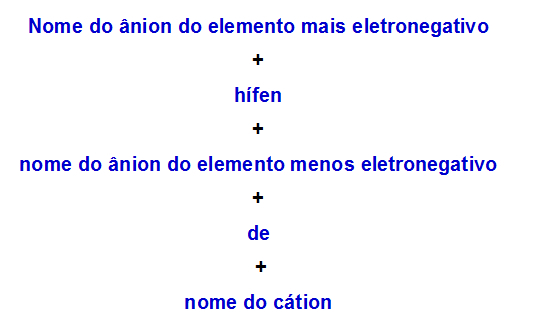
Nomenklaturregel brukt for dobbeltsalter med to anioner
Her er to eksempler på bruk av denne regelen:
Første eksempel: MgFI
Dette saltet består av:
Kation: magnesium (Mg+2);
Mest elektronegative anion: fluor (F-1);
Mindre elektronegativ anion: jodid (I-1).
Derfor heter navnet magnesiumfluoridjodid.
Andre eksempel: ZnNO2br
Dette saltet består av:
Kation: sink (Zn+2);
Mer elektronegativ anion: nitritt (NO2-1);
Mindre elektronegativ anion: bromid (Br-1).
Derfor er navnet sinksnitritbromid.
Montering av formelen til et dobbelt salt fra nomenklaturen
a) For dobbelt salt med to kationer
Konstruksjonen av formelen til a dobbelt salt det avhenger av å kjenne navnet, som er standardisert som i alt salt, det vil si først kationen og deretter anionet. Siden dobbeltsaltet kan ha to kationer, følger deres rekkefølge og plassering i formelen det gitte navnet.
Første eksempel: barium nikkel pyrofosfat II
Dette saltet inneholder fosfat (P2O7), barium (Ba+2) og nikkel II (Ni+2), kationer skrevet i den sekvensen. Så formelen er BaNiP2O7.
Andre eksempel: kobber II fosfat og gull I
Dette saltet har fosfat (PO4-3), kobber II (Cu+2) og gull I (Au+1), kationer skrevet i den sekvensen. Derfor er formelen CuAuPO4.
b) For dobbelt salt med to anioner
I tilfelle dobbelt salt med to anioner følger vi også når vi plasserer anionene i formelen, rekkefølgen slik de vises i det gitte navnet.
Første eksempel: nikkel sulfat-jodid III
Dette saltet har sulfationer (SO4-2) og jodid (I-1), skrevet i denne sekvensen, og nikkel III-kationen (Ni+3). Så formelen er NiSO4JEG.
Andre eksempel: blycyanidfosfat IV
Dette saltet har fosfatanioner (PO4-3) og cyanid (CN-1), skrevet i denne sekvensen, og blykation IV (Pb+4). Så formelen er PbPO4CN.
Av meg. Diogo Lopes Dias
Kilde: Brasilskolen - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-um-sal-duplo.htm

