Du såper og vaskemidler brukes til å fjerne smuss og spesielt fett fra materialer. Men hva er forskjellen mellom de to? Er det mer fordel å bruke såpe eller vaskemiddel? Hva med miljøet? Hvilket forurenser mindre?
La oss se på strukturen til hver enkelt for å komme til et tilfredsstillende svar.
Såper har følgende typiske struktur:
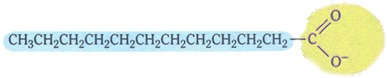
Typisk struktur for såper.
Merk at den har en ikke-polær del, representert av fargen blå, som samhandler med fett og olje, som også er upolær; og har en polær del (i gult), som samhandler med vann.
Strukturen til vaskemidler har også en polær og en ikke-polær del, som du kan se nedenfor:
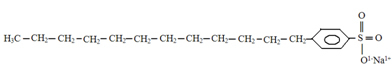
Typisk struktur for vaskemidler.
Poenget vi vil trekke oppmerksomhet mot, og som kan observeres ved å sammenligne de to strukturene, er at de vanligste vaskemidlene er salter avledet fra svovelsyre (H2KUN4), som er en sterk syre og gir mer skade på miljøet. Derfor er det tilstedeværelse av svovel (S) i vaskemiddelstrukturen. Det grunnleggende råmaterialet til vaskemidler er Petroleum, som er en ikke fornybar fossil energiressurs.
I tillegg er saken vist ovenfor et biologisk nedbrytbart vaskemiddel, men det er noen vaskemidler, som er de som har forgreninger i strukturen, som ikke er biologisk nedbrytbare, eller det vil si at de ikke brytes ned av mikroorganismer, og hvis de dumpes i elver og innsjøer, kan det forårsake alvorlige miljøeffekter med den påfølgende død av forskjellige fisker, alger, insekter og fugler vannlevende.
Såper er laget av oljer eller fett som reagerer med en sterk base, som f.eks natriumhydroksid (NaOH). Såper er såpe karboksylsyresalter, som er svake syrer. I strukturen til disse såpene erstattes hydrogenet fra karboksylgruppen (─COOH) med natriumioner (Na+), kalium (K+) eller ammonium (NH4+), som vist under. Resultatet er at alle såper er biologisk nedbrytbare.
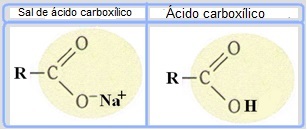
Såper er salter av karboksylsyrer der hydrogenet i syren erstattes av et kation.
En annen ulempe med vaskemidler er at mange av dem inneholder fosfationer i sin struktur. Disse ionene brukes av alger som næringsstoffer, så når disse vaskemidlene blir dumpet i elver har deres fosfationer økt drastisk, og disse algene formerer seg i stort antall. skala. Denne prosessen kalles eutrofiering og forårsaker fiskenes og andre vannlevende vesens død, da algene vil dekke overflatene til innsjøene, og forhindre at lys og oksygen kommer inn i vannet.
Og dermed, hvis vi ser på miljøspørsmålet, er bålsåpe det beste alternativet.

Overdreven algblomstring kalles eutrofiering.
Men hva med effektivitet?
Såper har en ulempe når rengjøring gjøres med vann som inneholder kalsium, magnesium og jernkationer, som anionene i såper kan reagere med disse kationene, med opprinnelse av uoppløselige forbindelser, som utfelles og danner det såkalte vannet hard. Som et resultat kan såper ikke fjerne smuss og fett.
Vaskemidler har derimot fordelen fremfor såper at de aldri reagerer med kationene i hardt vann og derfor renser uavhengig av vannet som brukes.
Jennifer Fogaça
Uteksamen i kjemi
Kilde: Brasilskolen - https://brasilescola.uol.com.br/quimica/sabao-x-detergente.htm

