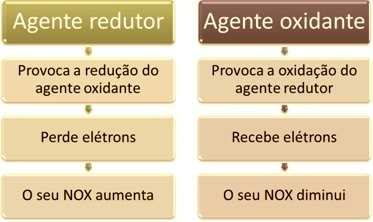
En av hovedtrekkene som skiller en oksidasjonsreduksjonsreaksjon (eller redoks) av de andre er tilstedeværelsen av et oksidasjonsmiddel og et reduksjonsmiddel, som kan defineres som følger:
Se for eksempel på den kjemiske reaksjonen nedenfor der aluminium (Al) korroderer i vandig saltsyre (HCl). Aluminiumatomer overfører elektroner til H-kationer+(her) og produsere Al-kationen3+(her):
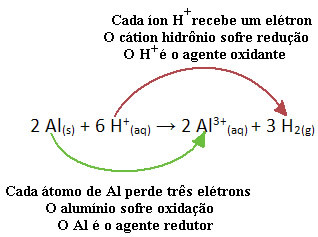
Merk at siden Al overførte elektroner, betyr dette at han forårsaket reduksjonen av H-kationene+(her); det er derfor han blir kalt reduksjonsmiddel. Allerede kationen H+(her) fjernet elektronene fra aluminiumet, forårsaker oksidasjon av det metallet; derfor fungerer han som en oksidasjonsmiddel.
I hverdagen er det mange eksempler på ytelsen til oksidasjonsmidler og reduksjonsmidler. Se på noen av dem og husk imidlertid at reduksjonen i alle tilfeller skjer samtidig med oksidasjonen; derfor, hvis det er et reduksjonsmiddel, er det også et oksidasjonsmiddel.
- Eksempler på reduksjonsmidler:
- I fotografiske filmer: fotografiske filmer inneholder lysfølsomme sølvsalter. På punkter der det er forekomst av lys er det en reduksjon av Ag-ioner +, noe som resulterer i kontrasten observert i negativene.

- Vitamin C: Vitamin C (L-askorbinsyre) er et kraftig reduksjonsmiddel i vandig løsning. Det har et eksepsjonelt anlegg for å bli oksidert, og det er derfor det er mye brukt, spesielt i matvarer som en antioksidant, det vil si at den tilsettes andre matvarer og beskytter dem mot mulig oksidasjon på grunn av sin egen ofre. Et eksempel er frukt som epler og pærer som mørkner i kontakt med oksygen i luften fordi de oksiderer. Men når du tilsetter en liten mengde appelsin- eller sitronsaft (som inneholder vitamin C) i frukten kuttet, forhindrer dette at denne reaksjonen oppstår, fordi C-vitamin virker som et reduksjonsmiddel og oksiderer før frukten.

- Hydrogengass: hydrogengassen (H2) brukes i rakettfremdrift og regnes som et av de viktigste energialternativene, da forbrenningen frigjør en stor mengde energi og ingen forurensende stoffer. I denne reaksjonen virker hydrogen som et reduksjonsmiddel og oksyderes av oksygen.
- Eksempler på oksidasjonsmidler:
- Ved produksjon av eddik: når vin utsettes for luft, blir den til eddik, hvor hovedkomponenten er eddiksyre. Dette er fordi etylalkoholen eller etanolen som er tilstede i vin oksiderer ved kontakt med atmosfærisk oksygen, noe som resulterer i eddiksyre. Dermed er oksygen et oksidasjonsmiddel. Selv opprinnelsen til begrepet "oksidasjon" er relatert til reaksjonen med oksygen.

- I rusten: som angitt i forrige eksempel, fungerer oksygen som et oksidasjonsmiddel for alkohol; og det gjør dette også i kontakt med forskjellige metaller, for eksempel jern, og forårsaker rustprosessen. I tillegg til oksygen i luften, er andre oksidasjonsmidler i dette tilfellet vann eller en sur løsning.
- I blekemidler: blekeeffekten av blekemiddel skyldes tilstedeværelsen av følgende to reduksjonsmidler: o hypoklorittanion (vanligvis i form av natriumsalt - NaOCl), til stede for eksempel i blekemiddel; og hydrogenperoksyd (H2O2), markedsført som hydrogenperoksid. Disse to forbindelsene har en veldig sterk tendens til å oksidere og forårsake reduksjon av andre kjemiske arter. Derfor er de ansvarlige for oksiderende stoffer som gir produkter mørk farge. For eksempel brytes lignin ned i cellulose og blir lettere og mer smidig. I tilfelle flekkfjerning og stoffbleking forårsaker disse oksidasjonsmidlene oksidasjon av organiske molekyler som fett og fargestoffer.

- I åndedrettsvern: en enkel engangs åndedrettsvern består av et klart rør som inneholder en vandig løsning av dikromatsaltet av kalium og silika, fuktet med svovelsyre; blandet med oransje farge. Dette saltet, i kontakt med alkoholdampen som er inne i den berusede sjåførens pust, reagerer og endrer fargen til grønn. Dette betyr at oksidasjon av etanol (alkohol) til etanol er forårsaket.

Av Jennifer Fogaça
Uteksamen i kjemi
Kilde: Brasilskolen - https://brasilescola.uol.com.br/quimica/conceito-exemplos-agente-redutor-agente-oxidante.htm
