Til nitrogenfunksjoner er en gruppe av organiske forbindelser som har atomer av nitrogen festet til karbonkjeden. De kjennetegnes ved sine respektive funksjonelle grupper, som er sett med atomer koblet i en viss konfigurasjon og som definerer de karakteristiske egenskapene til hver funksjon.
Nitrogenfunksjonene er:
aminer;
amider;
nitroforbindelser;
nitriler;
isonitriler.
Les også:Hva er oksygenfunksjonene?
Oppsummering av nitrogenfunksjoner
Nitrogenfunksjoner er organiske forbindelser som inneholder atomer av nitrogen.
Aminer, amider, nitroforbindelser, nitriler og isonitriler er nitrogenfunksjonene.
Uorganiske funksjoner kjennetegnes ved deres funksjonelle gruppe.
Aminer er avledet fra substitusjon av hydrogener av ammoniakk ved alkylradikaler.
Amider har samme karbonatom knyttet til nitrogen og karbon. oksygen.
Nitroforbindelser inneholder -NO-gruppen.2.
Nitriler er karakterisert ved tilstedeværelsen av en trippelbinding mellom karbon og nitrogen.
Isonitriler har en trippelbinding mellom nitrogen og karbon, med nitrogen festet til karbonkjeden.
Videoleksjon om nitrogenholdige funksjoner
Hva er nitrogenfunksjoner?
Nitrogenfunksjoner er et sett av organiske funksjoner som har nitrogenatomet i sin struktur, i tillegg til karbon- og hydrogenatomer. De er: aminer, amider, nitroforbindelser, nitriler og isonitriler,
Det som skiller de nitrogenholdige funksjonene er de respektive funksjonelle gruppene, som er det strukturelle arrangementet av atomer som er ansvarlige for egenskapene til stoffet.
Hva er nitrogenfunksjonene?
aminer
Den organiske funksjonen gruven er karakterisert ved å binde minst en karbonkjede til nitrogenatomet. Den funksjonelle gruppen av aminer er -N-R1R2R3 (R-gruppene er karbonkjeder eller hydrogenatomer, hvorav minst én er en karbonkjede).

aminene er avledet fra ammoniakk (NH3), med ett eller flere hydrogenatomer erstattet med karbonatomer eller alkylligander. De er grunnleggende stoffer, forlater pH større enn 7 i vandig løsning.
De er klassifisert i henhold til mengden hydrogenatomer erstattet av karbonligander (alkyl- eller arylgrupper), som kalles substituenter.
- Primære aminer: har en enkelt karbonsubstituent.
- Sekundære aminer: har to karbonsubstituenter.
- Tertiære aminer: har tre karbonsubstituenter, det vil si at nitrogenatomet ikke lenger er bundet til noe hydrogenatom, og etablerer tre Tilkoblinger enkel med karbonatomer.
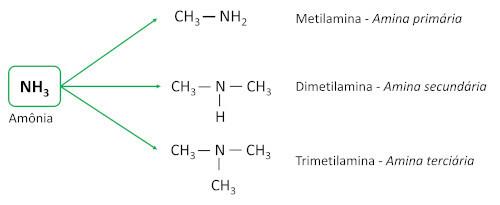
EN nomenklatur for aminer følger retningslinjene til IUPAC (International Union of Pure and Applied Chemistry). Når det gjelder primære aminer, tar konstruksjonen av navnet hensyn til antall karboner (prefiks), arten av bindingen mellom karboner (infiks) og begrepet brukes gruven for suffikset (slutten av ordet).

Se eksempelet:
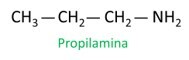
Når du tilordner tall til karbon for plasseringen av radikaler, tilordne lavest mulig tall til atomet nærmest NH-gruppen.2.
For sekundære og tertiære aminer vurderer nomenklaturen den lengste substituentgruppen festet til nitrogenet som hovedkjede, og de andre ligandene er skrevet med prefikset som refererer til antall karboner og suffikset -il, med bokstaven N foran seg.

Eksempel:
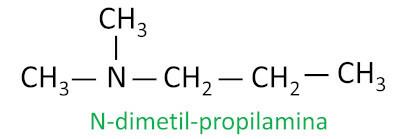
Amider
Den organiske funksjonen amid karakteriseres av binde en karbonylgruppe (C=O) til nitrogenatomet, hvor nitrogen kan bindes til karbon- eller hydrogenatomer.
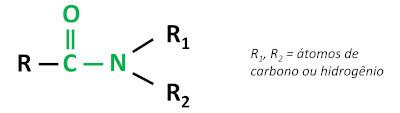
amidene er grunnleggende stofferog etterlater pH over 7 i vandig løsning. Stoffet urea tilhører gruppen amider og er en forbindelse som er naturlig tilstede i urin, avledet fra nedbrytningsprosesser som skjer i levende organismer.
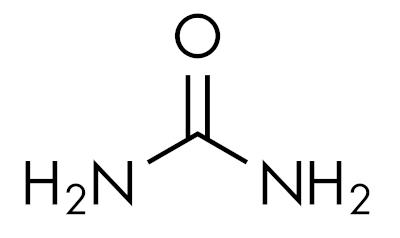
Amider er karakteristiske avhengig av nivået av nitrogensubstitusjon. Som dette:
- Primære amider: holder to hydrogenatomer sammen med nitrogen.
- Sekundære amidereller monosubstituert: en av hydrogenene er erstattet av karbonkjede, så nitrogen opprettholder en enkeltbinding med hydrogen.
- tertiære amidereller fortrengt: Nitrogen har ikke lenger hydrogenbindinger, som alle er erstattet av karbon.

Amider er Navngitt i henhold til IUPAC, molekylene blir navngitt av sekvensen:

I forgrenet amid deltar karbonatomet i amidgruppen i hovedkjeden, og karbontallet må starte med det. Se:
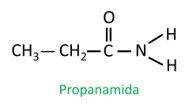 |
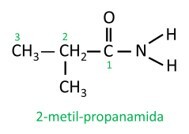 |
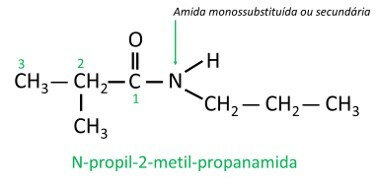
I monosubstituerte eller disubstituerte amider, bokstaven N indikerer posisjonen til grenen som er festet til nitrogenatomet. Hvis det er en annen radikal i kjeden, vil den bli skrevet etter å ha identifisert radikalen som refererer til N.
nitroforbindelser
Du nitroforbindelser er organiske forbindelser som inneholder en nitrogruppe (-NO2) festet til en karbonkjede, som kan være alifatisk (åpen eller lineær) eller aromatisk.
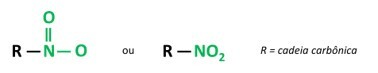
EN hovedkjennetegn ved disse stoffene er deres eksplosive kraft. Den eksplosive kapasiteten er assosiert med aromatiske nitroforbindelser, og jo større antall nitrogrupper, desto større er eksplosjonen. Alifatiske nitroforbindelser brukes i laboratorier som organiske løsemidler.
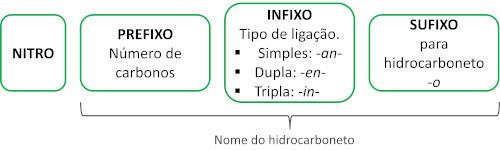
Nomenklaturen for disse forbindelsene er dannet av ordet nitro etterfulgt av navnet på hydrokarbon (prefiks + infiks + avslutning -O).
Se noen eksempler:
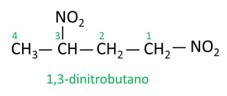 |
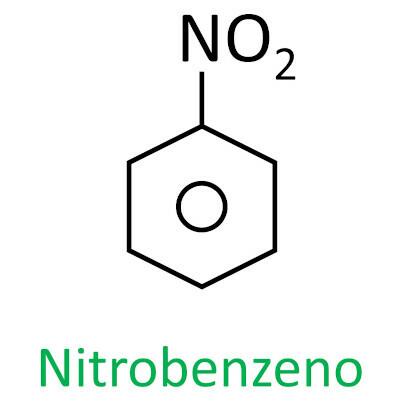 |
nitriler
Nitriler er organiske forbindelser preget av trippelbinding mellom et karbonatom og et nitrogenatom, som presenterer den funksjonelle gruppen – C ≡ N. I nitriler er nitrogenet i enden og karbonet er festet direkte til karbonkjeden.

nitrilene Også kjent som cyanider, da de stammer fra reaksjoner med blåsyre (HCN).
de er stoffer giftig for mennesker, fordi i kroppen kan de danne blåsyre i kontakt med magesyre, forhindre prosesser av cellulær respirasjon av cellene.
I naturen kan nitriler finnes i noen steinfrukter, men i svært lav konsentrasjon, uten risiko, og i bladene til vill kassava.

Iupac-regelen for nomenklaturen av nitriler definerer dette begrepet nitril legges til som et suffiks:

Se noen eksempler:
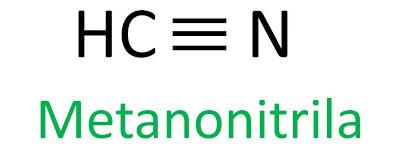 |
 |
Den vanlige formen for nomenklatur for nitriler er cyanid + radikalnavn.
isonitriler
Isonitriler, eller isonitriler, er forbindelser dannet av trippelbinding mellom et karbonatom og et nitrogenatom, som presenterer den funksjonelle gruppen – R ≡ C. I isonitriler er karbonet i enden og nitrogenet er festet direkte til karbonkjeden.

Isonitrilene skiller seg fra nitrilene på grunn av plasseringen av nitrogen- og karbonatomene, og I isonitriler er nitrogen karakterisert som et heteroatom., da den er plassert mellom to karboner.
De er ustabile arter og kan omdannes til nitriler ved høye temperaturer. Isocyanidinsyrereaksjoner gir opphav til isonitriler, som er grunnen til at disse forbindelsene også er kjent som isocyanider.
Isonitrilmolekyler følger Iupac-regelen for navngivning:
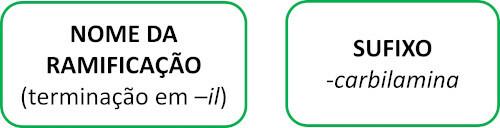
Se noen eksempler:
 |
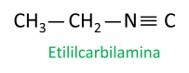 |
Anvendelser av nitrogenfunksjoner
Stoffene som tilhører de nitrogenholdige funksjonene har mange bruksområder, hovedsakelig i industriområdet, for fremstilling av polymerer, gummi, syntetiske fibre, legemidler, landbrukskjemikalier, plantevernmidler og eksplosiver.
Til aminer brukes i produksjonen av fargestoffer, såper, narkotika, i ferd med gummivulkanisering, eksplosiver og andre industrielle prosesser, og finnes også i planter og dannes i nedbrytningsprosesser for organisk materiale.

Til amider har bred anvendelse i industri- og kjemisk sektor, som er tilstede i produksjonen av polymerer (som nylon og polyuretan), harpikser, eksplosiver, gjødsel, insektmidler, gjødsel og narkotika.

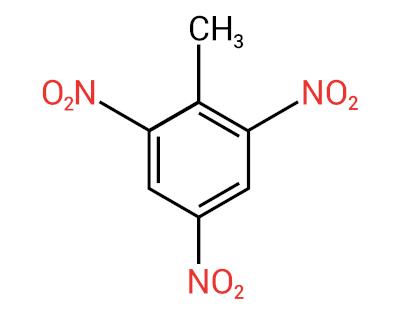
Du nitroforbindelserHovedapplikasjonen er produksjon av eksplosiver. som brukes i militær, industri og metallurgisk sektor (for råvareutvinning). En av de mest kjente nitroforbindelsene er trinitrotoluen, populært kjent som TNT. Andre anvendelser av nitroforbindelser er i produksjon av plantevernmidler, bakteriedrepende midler, fargestoffer, petroleumsraffinering, etc.

Til nitriler brukes som organiske løsemidler i laboratoriet og i industrien, deltar i utvinnings- og produksjonsprosessene av noen syntetiske fibre, plastpolymerer, fargestoffer og gjødsel.

Til isonitriler brukes i ulike prosesser for produksjon av organiske forbindelser, slik som løsemidler, og delta i produksjonen av landbrukskjemikalier, plantevernmidler, gummi og plast.
Les også:Halogenider - stoffer som har halogenatomer knyttet til karbonkjeden
Løste øvelser om nitrogenfunksjoner
Spørsmål 1
(FPS-PE-modifisert) Anvendelsen av nitrogenholdige forbindelser i syntetisk organisk kjemi er svært diversifisert og involverer fremstilling av medikamenter, fargestoffer, eksplosiver og vitaminer. Se på forbindelsene nedenfor.
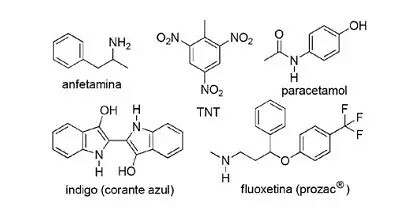
Om disse forbindelsene, merk den uriktige påstanden.
a) TNT er en nitroforbindelse.
b) Den nitrogenholdige delen av fluoksetin er et sekundært amin.
c) Amfetamin er klassifisert som et primært amid.
d) Indigo har heteroaromatiske ringer i sin struktur.
e) Den nitrogenholdige delen av paracetamol er et amid.
Vedtak:
Bokstav C
Gjenstanden De er riktig, fordi TNT er en nitroforbindelse fordi den har INGEN grupper2.
Gjenstanden B er korrekt. Den nitrogenholdige delen av fluoksetin er et sekundært amin fordi det er knyttet til to karbonsegmenter.
Gjenstanden w er feil, da amfetamin er klassifisert som et primært amin, ikke et amid. Merk at den nåværende gruppen er NH2. Så dette er kjernen i spørsmålet.
Gjenstanden d er riktig, siden indigo har heteroaromatiske ringer i strukturen, det vil si ringer dannet av karbonatomer og et annet element - i dette tilfellet nitrogen.
Gjenstanden Det er er riktig, fordi paracetamol er et amid som presenterer karbon knyttet til nitrogen og oksygen.
spørsmål 2
(UFMS) Yerba mate (Ilex paraguariensis), opprinnelig fra Sør-Amerika, brukes som en styrkende og stimulerende drikk. Produktet oppnådd ved å behandle yerba mate-blader kan brukes til å forberede chimarrão og tereré, blant andre drikker som vanligvis og kulturelt konsumeres i regioner i Argentina, Paraguay og Brasil. Den store interessen for yerba mate skyldes de kjemiske forbindelsene som finnes, på grunn av dens antioksidant-, stimulerende og vanndrivende egenskaper.
(Tilgjengelig i: http://repositorio.utfpr.edu.br/jspui/bitstream/1/3158/1/PG_PPGEP_Henrique%2C%20 Flavia%20Aparecida_2018.pdf. Tilgang: 01. nov. 2018. Tilpasset).
De stimulerende egenskapene til yerba mate er relatert til innholdet av metylxantiner, en av de viktigste er koffein, struktur presentert nedenfor:

Når man analyserer strukturformelen til koffein, er det riktig å si at det har følgende organiske funksjoner og egenskaper:
a) aldehyd og amid, basisk.
b) amin og amid, alkalisk.
c) amin og keton, alkalisk.
d) keton og amid, amfotere.
e) karboksylsyre og amin, basisk.
Vedtak:
Bokstav B
Ved å analysere koffeinstrukturen identifiseres amin- og amidfunksjonelle grupper, som fremhevet i bildet nedenfor. Siden disse to gruppene har en basisk eller alkalisk egenskap, har koffein også denne egenskapen, noe som betyr at vandige koffeinløsninger har en pH over 7.
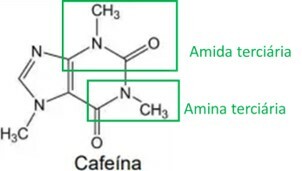
Av Ana Luiza Lorenzen Lima
Kjemilærer
Kilde: Brasil skole - https://brasilescola.uol.com.br/quimica/funcoes-nitrogenadas.htm
