EN sublimering Det er en endring i den fysiske tilstanden til stoffet preget av direkte passasje fra fast fase til gassfase, uten å passere gjennom væskefasen. Strengt tatt kan ethvert stoff gjennomgå sublimering, men under spesifikke forhold med trykk og temperatur. Sublimering er korrelert med damptrykket i den faste fasen, så vel som med de intermolekylære interaksjonene som utøves av de faste stoffene.
Denne prosessen kan lett observeres i et stykke tørris, som består av fast karbondioksid. Karbondioksid sublimeres under trykk og ved romtemperatur. Den motsatte prosessen til sublimering kan kalles resublimering eller avsetning. For at sublimering skal skje, må materie absorbere energi, så det regnes som en endoterm prosess.
Les også: Hva er materiens fysiske tilstander?
Emner i denne artikkelen
- 1 - Sammendrag om sublimering
- 2 - Hva er sublimering?
-
3 - Drift av sublimering
- Hva er damptrykk?
- Damptrykk og sublimering
- Fasediagram
- 4 - Eksempler på sublimering
- 5 - Løste øvelser om sublimering
Sammendrag om sublimering
Sublimering er den direkte passasjen fra fast fase til gassfase, uten å gå gjennom væskefasen.
Spesifikke forhold for trykk og temperatur er nødvendige for å observere sublimeringen av et stoff.
Sublimering påvirkes av termodynamiske aspekter, som damptrykk i fast fase og intermolekylære interaksjoner.
Sublimering er en endoterm prosess.
Et eksempel på sublimering er det som skjer i tørris, som består av fast karbondioksid.
Hva er sublimering?
sublimering er den direkte overgangen fra fast fase til gassfaseuten å gå gjennom væskefasen. Det oppstår under spesifikke temperatur- og trykkforhold for noen faste stoffer. Denne overgangen er en fysisk prosess med tilstandsendring, som ikke involverer kjemiske reaksjoner.
Den omvendte prosessen, dvs. den direkte passasjen fra gassfasen til fast fase, kalles på forskjellige måter. Noen forfattere beholder ordet sublimering for denne faseendringen, mens andre bruker "resublimering" og til og med "avsetning".
Ikke stopp nå... Det er mer etter publisiteten ;)
Hvordan sublimering fungerer
En parallell kan trekkes mellom sublimering og fordampning. I begge tilfeller er endepunktet gassfase. Forskjellen er åpenbart i startfasen: faststoff for sublimering og væske for fordampning.
I begge tilfeller, det er påvirkning av trykk devapor og også termodynamiske aspekter, som involverer varme og intermolekylære interaksjoner.
Hva er damptrykk?
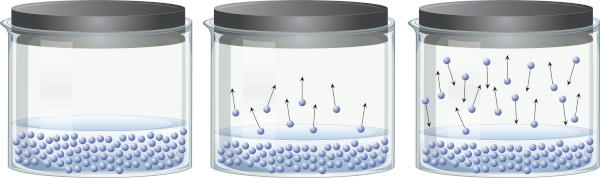
I en lukket beholder som inneholder en væske, er det mulig å oppfatte at det er en likevekt mellom væskefasen og dampfasen. Dette skjer fordi, selv under koketemperaturen, er energien som er tilstede tilstrekkelig til at noen molekyler av væsken løsner og passerer inn i dampen. Noen dampmolekyler kan imidlertid også kondensere igjen og gå tilbake til væskefasen, noe som demonstrerer reversibiliteten til prosessen.
Denne dampen er laget av materie (har masse og volum), øvelser trykk på overflaten av væsken, kjent som damptrykk. Det er ikke avhengig av væskemengden, men av temperaturen, fordi jo høyere temperatur, jo lettere løsnes molekylene fra væskefasen.
Væsker som har høyt damptrykk ved vanlige temperaturer kalles flyktige. For eksempel, ved 25°C har etyleter et damptrykk på 0,58 atm, aceton (propanon) har et damptrykk på 0,29 atm, mens vann har et damptrykk på 0,023 atm. Forresten, når damptrykket er identisk med atmosfærisk trykk, koker væsken. For å lære mer om damptrykk, klikk her.
Damptrykk og sublimering
Selv om det er i mindre grad, faste stoffer har også damptrykk, men mye lavere enn for væsker. For eksempel, selv ved en temperatur på 1000 K, er damptrykket til jern bare 9,21 x 10-20 atm. Noen faste stoffer klarer imidlertid å gjennomgå sublimering, for eksempel jod, og presenterer et høyere damptrykk ved normale temperaturer (4 x 10-4 atm).
Dette er bare mulig med passasje av molekyler fra fast tilstand direkte til gassform. For at dette skal skje, må molekyler av faststoffet må tilstede intermolekylære interaksjoner svak (i jod er de for eksempel av typen indusert dipol-indusert dipol).
Det ser man også sublimeringsprosessen er endoterm, det vil si at det er behov for at molekylene til det faste stoffet absorberer energi i form av varme slik at de kan bryte de intermolekylære interaksjonene og gå over i damptilstanden. Mengden varme som er involvert kan måles med en termodynamisk mengde kjent som sublimeringsentalpien.
Fasediagram
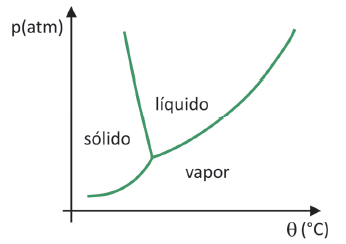
Til å vite i hvilket trykk- og temperaturområde sublimeringen av et fast stoff vil skje, må du evaluere fasediagrammet ditt. La oss se på tilfellet med karbondioksid, CO2.

I et fasediagram samler grenselinjene mellom tilstander (fast, væske og gass) trykk- og temperaturverdiene for det skjer en tilstandsendring. Når man observerer tilfellet med CO2, legges det merke til at ved 1 atmosfære trykk, går den faste fasen direkte til dampfasen ved en temperatur på -78,5 °C, noe som karakteriserer en sublimering.
Karbondioksid har bare en flytende fase ved trykk over 5,11 atmosfærer, og utover det trykket er sublimering ikke lenger mulig. For å lære mer om fasediagrammet, klikk her.
eksempler på sublimering
Tørris: tørris, ofte brukt til å lage tåkeeffekter på fester og arrangementer, er faktisk karbondioksid i fast form.

møllkuler: møllkuler er laget av naftalen, en aromatisk organisk forbindelse. Det brukes for å fjerne vond lukt og også skremme bort møll, kakerlakker og andre giftige dyr, og det er derfor det er vanlig at de brukes i skap eller til og med urinaler.

Kamfer: Med en karakteristisk lukt kan kamferstein også gjennomgå sublimering. De tjener også til å skremme bort mygg og forhindre mugg.

Jod: ikke-metallet som tilhører halogenene, gjennomgår også sublimering.

Imidlertid, blant stoffene som presenteres, bare karbondioksid gjennomgår sublimering under omgivelsesforhold. De andre, selv med sublimering, kan gjennomgå normal fusjon under trykket vi lever i.
Les også: Plasma - den fjerde tilstanden av materie
Løste øvelser om sublimering
Spørsmål 1
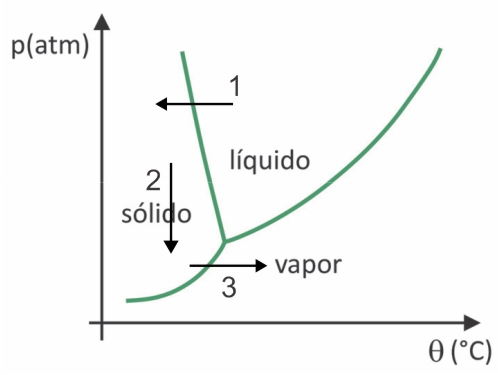
(Fuvest 2020) I supermarkeder er det vanlig å finne såkalt frysetørket mat, som frukt, grønnsaker og kjøtt. Frysetørket mat er fortsatt egnet for konsum etter lang tid, selv uten kjøling. Begrepet "lyofilisert" i disse matvarene refererer til fryseprosessen og påfølgende dehydrering ved vannsublimering. For at sublimering av vann skal skje, kreves en kombinasjon av forhold, som vist i trykk-temperatur-grafen, hvor linjene representerer faseoverganger.
Til tross for at det er en prosess som industrielt krever bruk av viss teknologi, er det bevis på at folk pre-columbianere som bodde i de høyeste områdene i Andesfjellene var i stand til å frysetørr mat, noe som gjorde det mulig å lagre den for mer tid. Sjekk alternativet som forklarer hvordan den naturlige frysetørkeprosessen skjedde:
a) Sublimering av vann skjedde på grunn av lave temperaturer og høyt atmosfærisk trykk i fjellet.
b) Mat, etter å ha vært naturlig frosset i kalde perioder, ble ført til den laveste delen av fjellene, hvor atmosfærisk trykk var lavere, noe som muliggjorde sublimering.
c) Maten ble eksponert for solen for å øke temperaturen, og det lave lokale atmosfæriske trykket favoriserte størkning.
d) Temperaturene var lave nok i de kalde periodene til å fryse mat, og det lave atmosfæriske trykket i høyfjellet gjorde sublimering mulig.
e) Matvarene, etter å ha vært naturlig frosne, ble presset for å øke trykket, slik at sublimering kunne skje.
Respons: Bokstav D.
Ved lyofilisering er det frysing av vann med påfølgende sublimering. Pre-columbianske folk kunne gjennomføre en slik prosess, da vannet om vinteren kunne fryse (pil 1) og med lavtrykket (pil 2) i de høyeste områdene i Andesfjellene, kan det gjennomgå sublimering (pil 3).
spørsmål 2
(Uerj 2005) Tørris, eller størknet karbondioksid, mye brukt i kjøleprosesser, gjennomgår sublimering under omgivelsesforhold. Under denne transformasjonen oppstår blant annet fenomenene energivariasjon og forstyrrelse av interaksjoner.
Disse fenomenene er klassifisert som henholdsvis:
a) eksoterm - interionisk
b) eksoterm - internukleær
c) isotermisk - interatomisk
d) endotermisk - intermolekylær
Respons: Bokstav D.
Sublimering er en endoterm prosess, siden den krever absorpsjon av varme for å forstyrre interaksjonene som holder fastfasemolekylene kompakte. Disse interaksjonene er av den intermolekylære typen.
Av Stefano Araujo Novais
Kjemilærer
Lær mer om dette fenomenet.
Svaret ligger i trykk- og temperaturendringer.
Lær om materiens fysiske tilstander og se hva de er. Lær også hva Bose-Einstein er og hvor vi kan finne materie i plasmatilstanden.
Induserte dipol-induserte dipolkrefter er de svakeste intermolekylære kreftene som oppstår mellom ikke-polare molekyler.
Se hvordan du identifiserer om et stoff har et høyere kokepunkt enn et annet ved forholdet mellom intermolekylære krefter og kokepunkt.