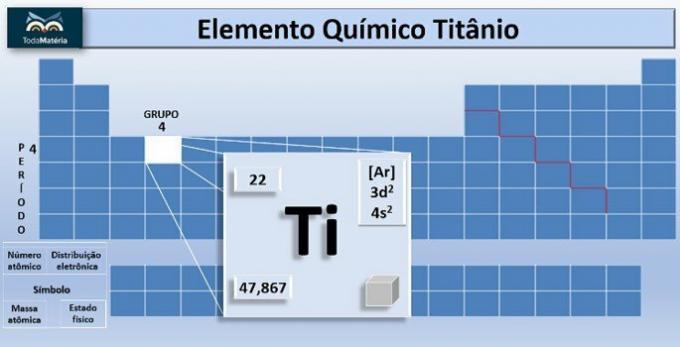
O titan er det kjemiske elementet med symbol Ti og atomnummer, det vil si antall protoner lik 22. Dette metallet er plassert i gruppe 4 og 4 i det periodiske systemet.
Atommassen til grunnstoffet er 47.867 u, og fordi det har 22 elektroner i atomets elektroner, er elektronfordelingen 1s2 2s2 2p6 3s2 3 s6 4s2 3d2.
Titan har ønskelige egenskaper for mange bruksområder siden det er like sterkt som stål og mye lettere.
Fordi det er et duktilt, ildfast, korrosjonsbestandig metall, har det mekanisk motstand, termisk stabilitet og lav reaktivitet, er det tilsatt metalllegeringer slik at de har en høy opptreden. Dens biokompatibilitet og ikke-toksisitet gjør den også nyttig for å lage beinproteser.
De viktigste egenskapene til titan er:
- Smeltepunkt: 1668 °C
- Kokepunkt: 3287 °C
- Tetthet: 4,5 g/cm3
- Farge: sølvgrå
- Fysisk tilstand ved 20 °C: fast
- Isotoper: Ti46, du47, du48, du49 og du50
Dette kjemiske elementet ble oppdaget av engelskmannen William Gregor i 1791 og navnet, avledet fra det greske titaner, ble senere tilskrevet av Martin Heinrich Klaproth.
Titan er det niende mest tallrike grunnstoffet på planeten og finnes i jordskorpen i malmer som rutil (TiO)2) og ilmenitt (FeTiO3). Derfor er gruvedrift hovedmetoden for å skaffe dette metallet.
Hva brukes titan til?
Fordi det er kjemisk ikke-reaktivt ved romtemperatur, lett støpes, har høy mekanisk og korrosjonsbestandighet, brukes titan som et strategisk metall.
Luftfarts- og romfartsindustrien er hovedbrukerne av titan for produksjon av deler, som turbin- og flykroppskomponenter. Andre bruksområder er produksjon av tannproteser, kirurgiske implantater og smykker.
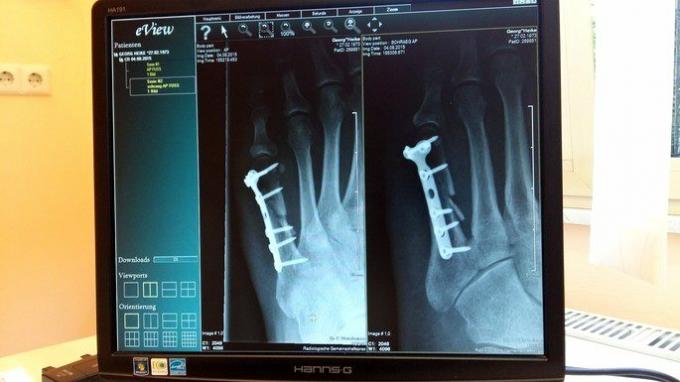
I medisin er titan veldig nyttig på grunn av dets kompatibilitet med menneskelig vev, letthet og styrke. Den brukes til produksjon av implantater til kroppsdeler, som fikseringsskruer, kneleddserstatning, humerusprotese, hofteprotese, blant annet.
Titandioksid (TiO2) er en av hovedforbindelsene til dette elementet, og brukes som blekemiddel. Vanligvis bruker hvitt blekk av høy kvalitet det til å forbedre det visuelle utseendet til farge og glans. Også andre produkter, som tannkrem og solkremer, bruker pigmentet. Det er også bruk som matfarge tilsatt i meieriprodukter, søtsaker og drikkevarer.
I arkitektur kan vi se bruken av titan for å dekke buede strukturer ved Guggenheim-museet i Bilbao, Nord-Spania.

I hverdagen kan vi finne en rekke produkter som har titan i sammensetningen, for eksempel sykkelrammer, briller og tennisracketer.
I kjemisk industri brukes titan som katalysator for reaksjoner. På denne måten gjør det mulig å kontrollere reaksjonshastigheten og redusere tiden for produktdannelse uten å påvirke sammensetningen av stoffene.
Bilindustrien har studert inkorporering av titan i produksjonen av biler for å redusere massen og dermed redusere drivstofforbruket og øke akselerasjonen.
Få mer kunnskap med innholdet:
- Kjemiske elementer
- Periodiske tabell
- Hva er metaller?
Bibliografiske referanser
ATKINS, P.W.; JONES, L. Prinsipper for kjemi: stille spørsmål ved moderne liv og miljø. 3.ed. Porto Alegre: Bookman, 2006.
FELTRE, R. Fundamentals of Chemistry: vol. enkelt. 4. utg. São Paulo: Moderna, 2005.
Lee, J. D. Ikke så kortfattet uorganisk kjemi. Oversettelse av 5. utg. Engelsk. Utgiver Edgard Blucher Ltd. 1999.


