Organiske forbindelser kan representeres på en rekke måter, for eksempel en flat strukturformel, en forenklet eller kondensert strukturformel eller en strekformel. Imidlertid er den enkleste representasjonen via molekylformelen.

Derfor, la oss se hvordan du bestemmer molekylformelen til organiske forbindelser, basert på de andre formlene nevnt ovenfor.
1. Gjennom den flate strukturformelen:denne formelen viser arrangementet eller arrangementet av atomer i molekylet. Nedenfor er for eksempel den flate strukturformelen til et av hydrokarbonene som finnes i bensin.

Merk at i denne formelen vises alle atomer og alle eksisterende bindinger mellom dem. Nå, for å bestemme molekylformelen til denne forbindelsen, tell bare antall atomer til hvert grunnstoff og plasser en indeks på nedre høyre side av det aktuelle elementet.
Et viktig aspekt å fremheve er det vi starter alltid molekylformelen til organiske forbindelser fra grunnstoffet karbon, da det er hovedbestanddelen av disse stoffene. Se eksempelet:
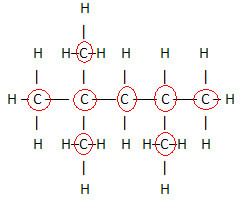
Siden det er 8 karboner, begynner vi å skrive molekylformelen slik: Ç8
For å fullføre denne formelen, teller vi mengden hydrogener:
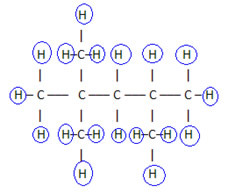
derfor din molekylær formel é Ç8H18.
2. Gjennom den forenklede eller kondenserte strukturformelen: i denne typen formel er mengden hydrogener forkortet. Se for eksempel på den samme formelen for molekylet som finnes i bensin, nå i en kondensert form:
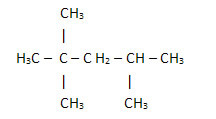
På denne måten er det enda enklere å telle mengden hydrogener, bare legg til indeksene (3 +3+ 3 +2 +1 +3 +3 = 18).
Men la oss nå se på den kondenserte strukturformelen til linolsyre, som finnes i grønnsaker som bomull, soyabønner, solsikker, etc. og som brukes i maling og lakk:
H3C─CH2CH2CH2CH2CH═CH─CH2CH═CH─CH2CH2CH2CH2CH2CH2CH2─COOH
Når vi teller mengden karbon, hydrogen og oksygen, har vi følgende molekylær formel av linolsyre: Ç18H32O2.
3. Gjennom slagformelen: denne formelen forenkler ytterligere hvordan man representerer organiske forbindelser, siden den utelater gruppene C, CH, CH2 og CH3.
Et eksempel er linolmolekylet, se hvordan det ser ut:

La oss telle mengden karbon først, og husk at i denne formelen er hver binding mellom karbonene representert med streken. Dermed tilsvarer spissene, samt de to bøyningspunktene, karbonatomer.
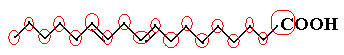
Så vi har: Ç18
Nå, for å telle mengden hydrogener, må vi huske at bindingene mellom karbon og hydrogen er underforstått, ettersom karbon er kjent for å lage fire bindinger; Dermed er mengden bindinger som mangler mengden hydrogen bundet til det elementet.
Se forklaringene nedenfor:
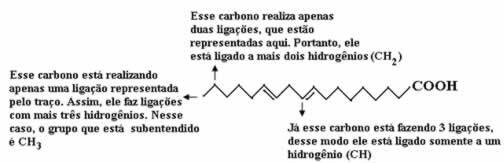
Dermed vil mengden hydrogener være: 32.

Mengden oksygen er ganske enkel å telle, da det bare er to. Siden molekylær formel é: Ç18H32O2.
Av Jennifer Fogaça
Uteksaminert i kjemi
Kilde: Brasil skole - https://brasilescola.uol.com.br/quimica/formulas-moleculares-compostos-organicos.htm



